Fosfolipidni sindrom je relativno česta patologija autoimunog porijekla. U pozadini bolesti često se uočavaju lezije krvnih sudova, bubrega, kostiju i drugih organa. U nedostatku terapije, bolest može dovesti do opasnih komplikacija sve do smrti pacijenta. Štaviše, bolest se često nalazi kod žena tokom trudnoće, što ugrožava zdravlje majke i djeteta.
Naravno, mnogi ljudi traže dodatne informacije postavljajući pitanja o uzrocima bolesti. Na koje simptome treba paziti? Da li postoji test na fosfolipidni sindrom? Može li medicina ponuditi efikasne tretmane?
Fosfolipidni sindrom: šta je to?
Ova bolest je prvi put opisana ne tako davno. Službene informacije o njemu objavljene su 1980-ih. Budući da je engleski reumatolog Graham Hughes radio na studiji, bolest se često naziva Hughesovim sindromom. Postoje i druga imena - antifosfolipidni sindrom i sindrom
Fosfolipidni sindrom je autoimuna bolest kod koje imuni sistem počinje proizvoditi antitijela koja napadaju vlastite fosfolipide u tijelu. Budući da su ove supstance dio membranskih zidova mnogih ćelija, lezije s takvom bolešću su značajne:
- Protutijela napadaju zdrave endotelne stanice, smanjujući sintezu faktora rasta i prostaciklina koji je odgovoran za širenje vaskularnog zida. U pozadini bolesti postoji kršenje agregacije trombocita.
- Fosfolipidi su takođe sadržani u zidovima samih trombocita, što dovodi do povećane agregacije, kao i brzog uništavanja.
- U prisustvu antitela, takođe se primećuje slabljenje aktivnosti heparina.
- Proces uništavanja ne zaobilazi ni nervne ćelije.
Krv se počinje zgrušavati u posudama, stvarajući krvne ugruške koji ometaju protok krvi, a time i funkcije različitih organa - tako se razvija fosfolipidni sindrom. Uzroci i simptomi ove bolesti interesuju mnoge ljude. Napokon, što se prije otkrije bolest, pacijent će razviti manje komplikacija.
Glavni razlozi za razvoj bolesti
Zašto ljudi razvijaju fosfolipidni sindrom? Razlozi se mogu razlikovati. Poznato je da pacijenti vrlo često imaju genetsku predispoziciju. Bolest se razvija u slučaju neispravnog rada imunološkog sistema, koji iz jednog ili drugog razloga počinje proizvoditi antitela na ćelije sopstvenog tela. U svakom slučaju, bolest mora biti nečim izazvana. Do danas su naučnici uspjeli identificirati nekoliko faktora rizika:
- Često se fosfolipidni sindrom razvija u pozadini mikroangiopatija, posebno trobocitopenije, hemolitičko-uremičnog sindroma.
- Faktori rizika uključuju i druge autoimune bolesti, poput lupus eritematozusa, vaskulitisa i sklerodermije.
- Bolest se često razvija u prisustvu malignih tumora u tijelu pacijenta.
- Faktori rizika uključuju zarazne bolesti. Infektivna mononukleoza i AIDS su posebno opasni.
- Protutijela se mogu pojaviti s diseminiranom intravaskularnom koagulacijom.
- Poznato je da se bolest može razviti uz uzimanje određenih lijekova, uključujući hormonalne kontraceptive, psihotropne lijekove, novokainamid itd.
Naravno, važno je otkriti zašto je pacijent razvio fosfolipidni sindrom. Dijagnostika i liječenje trebaju identificirati i, ako je moguće, ukloniti osnovni uzrok bolesti.
Oštećenje kardiovaskularnog sistema u fosfolipidnom sindromu
Krv i sudovi su prva "meta" koju napada fosfolipidni sindrom. Njegovi simptomi ovise o stupnju razvoja bolesti. Krvni ugrušci se u pravilu prvo stvaraju u malim žilama udova. Oni remete protok krvi, što je praćeno ishemijom tkiva. Pogođeni ud je na dodir uvijek hladniji, koža blijedi, a mišići postupno atrofiraju. Dugotrajna neuhranjenost tkiva dovodi do nekroze i naknadne gangrene.
Moguća je i duboka venska tromboza ekstremiteta koja je praćena pojavom edema, bolova i oštećenja pokretljivosti. Fosfolipidni sindrom može se zakomplicirati tromboflebitisom (upalom krvožilnih zidova), koji prati groznica, jeza, crvenilo kože na zahvaćenom području i akutni oštri bol.
Stvaranje krvnih ugrušaka u velikim posudama može dovesti do razvoja sljedećih patologija:
- aortni sindrom (praćen oštrim porastom pritiska u posudama gornjeg dijela tijela);
- sindrom (ovo stanje karakterizira oticanje, cijanoza kože, krvarenje iz nosa, dušnika i jednjaka);
- (praćeno poremećenom cirkulacijom krvi u donjem dijelu tijela, oticanjem udova, bolovima u nogama, zadnjici, trbušnoj šupljini i preponama).
Tromboza takođe utiče na rad srca. Često bolest prati razvoj angine pektoris, perzistentna arterijska hipertenzija, infarkt miokarda.
Oštećenje bubrega i glavni simptomi

Stvaranje krvnih ugrušaka dovodi do oštećenja cirkulacije krvi ne samo u udovima - pate i unutarnji organi, posebno bubrezi. S produženim razvojem fosfolipidnog sindroma moguć je takozvani infarkt bubrega. Ovo stanje prate bolovi u leđima, smanjenje količine urina i prisustvo nečistoća u njemu.
Krvni ugrušak može blokirati bubrežnu arteriju, što je praćeno jakim bolom, mučninom i povraćanjem. Ovo je opasno stanje - u odsustvu liječenja moguć je razvoj nekrotičnog procesa. Opasne posljedice fosfolipidnog sindroma uključuju bubrežnu mikroangiopatiju u kojoj se mali krvni ugrušci stvaraju direktno u bubrežnim glomerulima. Ovo stanje često dovodi do razvoja hronične bubrežne insuficijencije.
Ponekad postoji kršenje cirkulacije krvi u nadbubrežnim žlijezdama, što dovodi do kršenja hormonske pozadine.
Koji drugi organi mogu biti zahvaćeni?

Fosfolipidni sindrom je bolest koja pogađa mnoge organe. Kao što je već spomenuto, antitijela utječu na membrane živčanih ćelija, što ne može biti bez posljedica. Mnogi se pacijenti žale na uporne jake glavobolje, koje često prate vrtoglavica, mučnina i povraćanje. Postoji mogućnost razvoja različitih mentalnih poremećaja.
Kod nekih pacijenata krvni ugrušci nalaze se u posudama koje opskrbljuju vizuelni analizator. Dugotrajni nedostatak kiseonika i hranjivih sastojaka dovodi do atrofije optike. Tromboza retinalnih sudova moguća je uz naknadno krvarenje. Nažalost, neke od očnih patologija su nepovratne: oštećenje vida ostaje kod pacijenta cijeli život.
Kosti također mogu biti uključene u patološki proces. Reverzibilna osteoporoza često se dijagnosticira kod ljudi, sa deformacijama skeleta i čestim prijelomima. Opasnija je aseptična nekroza kostiju.
Oštećenja kože takođe su karakteristična za ovu bolest. Na koži gornjih i donjih ekstremiteta često se stvaraju paukove vene. Ponekad primijetite vrlo karakterističan osip koji izgleda poput malih, tačkastih krvarenja. Neki pacijenti razvijaju eritem na tabanima i dlanovima. Često se stvaraju potkožni hematomi (bez očiglednog razloga) i krvarenja ispod nokatne ploče. Dugotrajno kršenje trofizma tkiva podrazumijeva pojavu čira koji dugo zarastaju i teško se liječe.
Otkrili smo što je fosfolipidni sindrom. Uzroci i simptomi bolesti izuzetno su važna pitanja. Napokon, režim liječenja koji odabere liječnik ovisit će o tim čimbenicima.
Fosfolipidni sindrom: dijagnoza

Naravno, u ovom slučaju je izuzetno važno na vrijeme otkriti prisutnost bolesti. Liječnik može sumnjati na fosfolipidni sindrom čak i tokom anamneze. Prisustvo tromboze i trofičnih čireva, česti pobačaji i znakovi anemije kod pacijenta mogu potaknuti ovu ideju. Naravno, u budućnosti se vrše dodatni pregledi.
Analiza fosfolipidnog sindroma sastoji se u određivanju nivoa antitela na fosfolipide u krvi pacijenata. U opštoj analizi krvi možete primijetiti smanjenje nivoa trombocita, povećanje ESR-a, povećanje broja leukocita. Često sindrom prati hemolitička anemija, koja se može vidjeti i tokom laboratorijskih testova.
Uz to se vrši i krv. Kod pacijenata se opaža porast količine gama globulina. Ako je jetra oštećena u pozadini patologije, tada se povećava količina bilirubina i alkalne fosfataze u krvi. U prisustvu bubrežne bolesti može se primijetiti porast nivoa kreatinina i uree.
Za neke pacijente se preporučuju i specifični imunološki testovi krvi. Na primjer, mogu se obaviti laboratorijski testovi kako bi se odredio reumatoidni faktor i koagulant lupusa. S fosfolipidnim sindromom u krvi možete otkriti prisustvo antitela na eritrocite, povećanje nivoa limfocita. Ako postoje sumnje na ozbiljna oštećenja jetre, bubrega, kostiju, provode se instrumentalni pregledi, uključujući rendgen, ultrazvuk, tomografiju.
Koje su komplikacije bolesti?

Ako se ne liječi, fosfolipidni sindrom može dovesti do izuzetno opasnih komplikacija. U pozadini bolesti, u posudama nastaju krvni ugrušci, što je već samo po sebi opasno. Krvni ugrušci začepljuju sudove, remeteći normalnu cirkulaciju krvi - tkiva i organi ne dobijaju dovoljno hranljivih sastojaka i kiseonika.
Često, u pozadini bolesti, pacijenti razvijaju moždani udar i infarkt miokarda. Blokada žila ekstremiteta može dovesti do razvoja gangrene. Kao što je gore spomenuto, pacijenti imaju oštećenu bubrežnu i nadbubrežnu funkciju. Najopasnija posljedica je plućna embolija - ova se patologija razvija akutno i ne može se u svim slučajevima pacijent na vrijeme dostaviti u bolnicu.
Trudnoća kod pacijenata sa fosfolipidnim sindromom

Kao što je već spomenuto, fosfolipidni sindrom dijagnosticira se tokom trudnoće. Koja je opasnost od bolesti i šta učiniti u sličnoj situaciji?
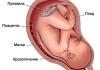
Zbog fosfolipidnog sindroma, u žilama nastaju krvni ugrušci koji začepljuju arterije koje dovode krv do placente. Embrion ne prima dovoljno kisika i hranjivih sastojaka, u 95% slučajeva to dovodi do pobačaja. Čak i ako se trudnoća ne prekine, postoji rizik od ranog odbacivanja posteljice i razvoja kasne gestoze, što je vrlo opasno i za majku i za dijete.
U idealnom slučaju, ženu treba testirati u fazi planiranja. Međutim, fosfolipidni sindrom se često dijagnosticira tokom trudnoće. U takvim je slučajevima vrlo važno na vrijeme uočiti bolest i poduzeti potrebne mjere. Antikoagulansi u malim dozama mogu se propisati budućoj majci. Pored toga, žena bi trebala biti podvrgnuta redovnim pregledima kako bi liječnik mogao na vrijeme primijetiti pojavu abrupcije posteljice. Svakih nekoliko mjeseci buduće majke prolaze kurs opće jačajuće terapije, uzimajući lijekove koji sadrže vitamine, minerale i antioksidante. Uz pravi pristup, trudnoće se često dobro završavaju.
Kako izgleda tretman?

Šta ako je osobi dijagnostikovan fosfolipidni sindrom? Liječenje je u ovom slučaju složeno i ovisi o tome ima li pacijent određene komplikacije. Budući da se krvni ugrušci stvaraju u pozadini bolesti, terapija je prvenstveno usmjerena na razrjeđivanje krvi. Režim liječenja obično uključuje upotrebu nekoliko grupa lijekova:
- Prije svega, propisani su indirektni antikoagulanti i antitrombocitna sredstva ("Aspirin", "Warfarin").
- Terapija često uključuje selektivne protuupalne lijekove nesteroidnog porijekla, posebno "Nimesulid" ili "Celekoksib".
- Ako je bolest povezana sa sistemskim eritemskim lupusom i nekim drugim autoimunim bolestima, liječnik vam može propisati glukokortikoide (hormonske protuupalne lijekove). Uz to se mogu koristiti imunosupresivni lijekovi koji potiskuju aktivnost imunološkog sistema i smanjuju proizvodnju opasnih antitela.
- Imunoglobulin se ponekad daje intravenozno trudnicama.
- Pacijenti povremeno uzimaju lijekove koji sadrže vitamine B.
- Za opći oporavak, zaštitu krvnih sudova i ćelijskih membrana, koriste se antioksidativni lijekovi, kao i lijekovi koji sadrže kompleks polinezasićenih masnih kiselina (Omacor, Mexicor).
Postupci elektroforeze povoljno utječu na stanje pacijenta. Kada je riječ o sekundarnom fosfolipidnom sindromu, važno je kontrolirati primarnu bolest. Na primjer, pacijenti s vaskulitisom i lupusom trebaju dobiti adekvatan tretman za ove određene patologije. Također je važno na vrijeme otkriti zarazne bolesti i provoditi odgovarajuću terapiju do potpunog oporavka (ako je moguće).
Predviđanja pacijenta
Ako je fosfolipidni sindrom dijagnosticiran na vrijeme i pacijent je dobio potrebnu pomoć, tada je prognoza vrlo povoljna. Nažalost, nemoguće je zauvijek se riješiti bolesti, ali uz pomoć lijekova moguće je kontrolirati njeno pogoršanje i provesti preventivni tretman tromboze. Situacije u kojima je bolest povezana sa trombocitopenijom i visokim krvnim pritiskom smatraju se opasnim.
U svakom slučaju, svi pacijenti kojima je dijagnosticiran fosfolipidni sindrom trebaju biti pod nadzorom reumatologa. Koliko puta se ponavlja analiza, koliko često trebate proći preglede kod drugih ljekara, koje lijekove trebate uzimati, kako nadgledati stanje vlastitog tijela - o svemu tome reći će vam ljekar.
Proučavam informacije o testovima koje treba obaviti. Iznos nije mali. Nakon čitanja ovog članka, odlučio sam da još neću uzimati ASK. Zasad ću predati samo hemostazu. Zanimljiv članak.
1. Definicija antifosfolipidnog sindroma (APS)
APS je klinički laboratorijski sindrom koji karakterizira arterijska ili venska tromboza / tromboembolija i / ili ponovljeni gubitak fetusa. Ovo stanje je posljedica prisustva antitijela na određene proteine \u200b\u200bplazme, koji su u mnogim slučajevima povezani sa fosfolipidima.
Uobičajeno je razlikovati primarni i sekundarni APS. Primarni APS se može uzeti u obzir ako se ovo stanje razvije u odsustvu drugih bolesti. Što se tiče sekundarne APS, ona se razvija u pozadini sistemskog eritemskog lupusa, drugih autoimunih bolesti, kao i u pozadini niza zaraznih bolesti, ili u slučaju uzimanja određenih lijekova.
2. Šta su antifosfolipidna antitela (APA)?
Trenutno postoje tri glavne vrste testova koji se koriste za otkrivanje AFA:
lupus antikoagulant (BA, sinonimi LA, lupus antikoagulant);
antitela na kardiolipin (ACL, sinonimi antikardiolipin, aCL, IgG aCL, IgM aCL);
kao i antitela na beta-2-glikoprotein-1 (anti-ß2-GPI).
Dakle, pojam antikoagulansa lupusa znači antitijela na proteine \u200b\u200bplazme, koja su najizravnije uključena u procese koagulacije krvi. Prisustvo ovih antitela ometa stvaranje određenih kompleksa tokom in vitro testa koagulacije, što zauzvrat povećava vreme koagulacije. U ovom slučaju govorimo o testovima kao što su aktivirano djelomično tromboplastinsko vrijeme (APTT, aPTT), Russell-ov test otrovne zmije (dRVVT), kaolinsko vrijeme i, mnogo rjeđe, protrombinsko vrijeme. VA se može otkriti izvođenjem testova zgrušavanja u tri koraka:
Sprovođenje analize krvi pacijenta, u kojoj se navodi povećanje vremena zgrušavanja.
Dodavanjem normalne plazme u omjeru 1: 1 u plazmu pacijenta nije moguće normalizirati vrijeme zgrušavanja. U ovom slučaju možemo govoriti o odsustvu nedostatka faktora koagulacije kod pacijenta, jer se u suprotnom vrijeme koagulacije vraća u normalu.
Normalizacija vremena zgrušavanja postiže se dodavanjem fosfolipida u plazmu pacijenta.
Posebno treba napomenuti da sve vrste probirnih testova na VA ni na koji način ne daju objektivne informacije o njegovom prisustvu u krvnoj plazmi pacijenta, te se stoga koriste isključivo u svrhu uzimanja uzoraka za prethodno opisana trostepena ispitivanja.
Recimo sada nekoliko riječi o antikardiolipinskim antitijelima, koja su antitijela na proteine \u200b\u200bplazme povezane sa fosfolipidima (poput istog kardiolipina). Moguće je otkriti antitela različitih klasa - IgG, IgA, IgM, a sadržaj takvih antitela naznačen je u "fosfolipidnim jedinicama" - GPL za IgG, MPL za IgM, kako je navedeno u međunarodnom referentnom standardu. U slučaju da se 2 ili više puta otkrije višak referentnog nivoa, tada možemo govoriti o pozitivnom rezultatu analize. U ogromnoj većini slučajeva, nivo iznad 40 jedinica GPL ili MPL smatra se pozitivnim. Do danas postoje dokazi o povezanosti između visokog nivoa IgG antitijela i tromboze, ali što se tiče vrijednosti izolirane detekcije IgM i IgA antitijela (tj. U nedostatku IgG antitela), to još uvijek nije jasno.
I konačno, što se tiče antitela na beta-2-glikoprotein-1, ona su, za razliku od anticardiolipinskih antitela, usmerena na protein koji nije povezan sa fosfolipidima. Ova vrsta analize je manje standardizovana od testova za VA ili ACL o kojima je ranije bilo reči.
3. Šta su antitela na fosfatidilserin (fosfatidilholin, fosfatidilinozitol, aneksin V) i možemo li razgovarati o APA ako ih pronađemo?
Tokom brojnih studija provedenih na ovom području, otkrivena su različita antitijela kod pacijenata sa APS-om, uključujući antitela na fosfatidilserin, fosfatidilinozitol, aneksin V. Trenutno, naučnici nisu spremni da opišu klinički značaj izolovanih (tj. Bez drugih APS ) ovih antitela. Sa negativnim AFA, gore navedena antitijela se takođe ne testiraju. Međutim, ako se utvrdi da pacijent ima "klasični" AFA, to mijenja ukupnu sliku i otkrivanje drugih antifosfolipidnih antitela u ovom slučaju ima određenu prognostičku vrijednost.
Pripreme + 10 nedelja + 20 nedelja + 30 nedelja + 36 nedelja
INR + 0,97 ± 0,08 + 0,91 ± 0,06 + 0,88 ± 0,07 + 0,87 ± 0,07
PTT (sekunde) + 27,0 ± 2,7 + 26,9 ± 2,7 + 27,1 ± 2,9 + 27,5 ± 2,8
Fibrinogen (g / L) + 4,13 ± 0,69 + 4,64 ± 0,84 + 5,39 ± 1,07 + 5,57 ± 1,13
Antitrombin III (%) + 101,5 ± 12,7 + 101,4 ± 10,3 + 104,2 ± 12,5 + 102,8 ± 13,5
Antitrombin III (U / ml) + + 1,02 ± 0,1 + 1,07 ± 0,14 + 1,07 ± 0,11
Protein C (%) + 99,4 ± 21,3 + 107,5 ± 24,9 + 99,3 ± 26,0 + 94,9 ± 25,5
Protein C (U / ml) + + 0,92 ± 0,13 + 1,06 ± 0,17 + 0,94 ± 0,2
Protein S (%) + 64,1 ± 15,8 + 62,1 ± 14,2 + 54,0 ± 13,3 + 51,7 ± 17,9
Protein S ukupno (U / ml) + + 0,83 ± 0,11 + 0,73 ± 0,11 + 0,77 ± 0,10
Protein Sw (U / ml) + + 0,26 ± 0,07 + 0,17 ± 0,04 + 0,14 ± 0,04
Protein Z (μg / ml) + + 2,01 ± 0,76 + 1,47 ± 0,45 + 1,55 ± 0,48
PTK (%) + + 120 ± 27 + 140 ± 27 + 130 ± 27
PAI-1 (U / ml) + 10,3 ± 4,7 + 11,3 ± 5,0 + 20,5 ± 7,3 + 22,4 ± 7,5
PAI-2 (mg / l) + + 31 ± 14 + 20,5 ± 7,3 + 22,4 ± 7,5
RFMK (nmol / L) + + 9,2 ± 8,6 + 11,8 ± 7,7 + 13,4 ± 5,2
D-dimer (μg / L) + + 91 ± 24 + 128 ± 49 + 198 ± 59
4. Na šta ukazuje otkrivanje antitela na kardiolipin (beta-2-glikoprotein-1, VA) u jednoj analizi?
U slučaju pojedinačnog otkrivanja AFA, postoji hitna potreba za potvrdom s intervalom od najmanje 8 tjedana, au nekim slučajevima se govori o intervalu od 12 tjedana. Ako se u najmanje dvije uzastopne analize, provedene u razmaku od najmanje 8 (12) tjedana, AFA otkriju u količini koja je najmanje 2 puta veća od referentnog nivoa, onda je to pouzdan pokazatelj njihovog prisustva.
5. Da li se AFA nalazi u zdravih ljudi?
Brojne studije pokazale su da se AFA može naći kod zdravih ljudi. Na primjer, u toku jedne studije, VA je otkrivena u 8% uzoraka zdravih davalaca, dok je LAC otkrivena u 1% uzoraka. Takođe treba napomenuti da je AFA češća kod žena nego kod muškaraca.
Također, AFA se može naći u zdravih trudnica sa nekompliciranom (normalnom) trudnoćom, a to se događa s frekvencijom od 0 do 11% (u većini slučajeva, u oko 2% slučajeva). Istovremeno, rezultati velikog pregleda prethodno sprovedenih studija, čiji je ukupan broj sudionika iznosio 14 000 ljudi, sugeriraju da se AFA otkriva u zdravih trudnica u 5% slučajeva.
6. Veza između prisustva AFA i nepovoljnih ishoda trudnoće
Moderna medicina poznaje sljedeće negativne ishode trudnoće kod pacijenata sa identificiranim AFA:
gubitak ploda nakon 10 tjedana trudnoće (a razlozi za to još nisu objašnjeni);
rana teška preeklampsija i eklampsija;
zaostajanje intrauterinog rasta.
Pored toga, neki istraživači ne isključuju povezanost AFA s ponovljenim (više od 3 puta) ranim pobačajima, međutim, nema jednoznačnog mišljenja, a drugi stručnjaci osporavaju ove podatke. Sigurno je reći da ne postoji veza između prisustva AFA i neplodnosti. Štaviše, rezultati sprovedene metaanalize pokazali su da je prethodno navedena hipoteza o mogućem uticaju AFA na neuspeh postupka vantelesne oplodnje (IVF) takođe neodrživa.
7. Opasnost API-ja za samu trudnicu
Kao što znate, trudnoća i porod su već faktor povećanog rizika od tromboze. Što se tiče APS-a, on dovodi do dodatnog povećanja ovog rizika, a taj je rizik vrlo varijabilan i ovisi o velikom broju različitih dodatnih čimbenika.
8. Da li je obavezno testiranje na AFA tokom trudnoće?
Ne, nema potrebe za skriningom na AFA za sve trudnice. Rezultati brojnih studija sugeriraju da nema utjecaja AFA na ishode prve trudnoće. Takođe, prisustvo AFA ne povećava rizik od nepovoljnog ishoda nakon jedne zamrznute trudnoće, pa stoga nije potrebna takva studija nakon jedne zamrznute trudnoće.
Sa preranim rođenjem zbog izražene intrauterine retardacije rasta u periodu kraćem od 34 tjedna;
Za prijevremene porođaje zbog teške preeklampsije (eklampsije) stare manje od 34 tjedna.
Što se tiče žena s pobačajima ili smrznutom trudnoćom u ranim (manje od 10 tjedana) periodima, u tim su slučajevima podaci o potrebi AFA studije donekle kontradiktorni. Većina stručnjaka sklona je mišljenju da sa jednom smrznutom u ranim fazama trudnoće nema potrebe za pregledom AFA. Ali s tri ili više uzastopno zamrznutih trudnoća u ranim fazama trudnoće, proučavanje AFA postaje prikladno.
Pored toga, preporučuje se testiranje na AFA u prisustvu kliničkih znakova APS-a prije trudnoće, koji uključuju slijedeća stanja:
neobjašnjiva tromboza i embolija;
moždani udar ili prolazni ishemijski napadi;
SLE;
hemolitička anemija;
neobjašnjiva trombocitopenija;
mesh livedo;
porodična istorija APS-a.
10. Možemo li govoriti o prisustvu API-ja u slučaju otkrivanja AFA (pozitivan rezultat u dvije uzastopne analize s razmakom od najmanje 8 tjedana)?
U ovom slučaju postoji definitivan odgovor - ne. Činjenica je da se dijagnoza određenog APS-a može postaviti samo uz kombinaciju kliničkih i laboratorijskih znakova.
Klinički znakovi APS uključuju:
tromboza, bezuvjetno potvrđena slikovnom ili histološkom metodom;
Gubitak fetusa u kasnoj trudnoći. U ovom slučaju mislimo na gubitak morfološki normalnog fetusa u periodu dužem od 10 tjedana, neobjašnjivo iz drugih razloga;
Jedan ili više prijevremenih trudova prije 34 tjedna zbog preeklampsije, eklampsije ili insuficijencije posteljice
Tri ili više uzastopnih fetalnih gubitaka u ranoj trudnoći (manje od 10 tjedana), a ti se gubici ne mogu objasniti hromozomskim abnormalnostima, kao ni anatomskim ili hormonalnim uzrocima majke.
Što se tiče laboratorijskih znakova APS-a, uobičajeno je razmotriti otkrivanje APS-a u 2 ili više uzastopnih analiza s razmakom od najmanje 8 (12) nedelja, ne pre 5 godina pre kliničke manifestacije:
antitela na kardiolipin (standardizovanom ELISA metodom) klase IgG i / ili IgM u visokom ili umerenom titru (više od 40 GPL ili MPL jedinica);
Antitela na beta-2-glikoprotein-1 (klase IgG ili IgM sa nivoom iznad 99. percentila za laboratorijske metode);
Lupus antikoagulant (metoda u 3 koraka).
U slučajevima kada postoji laboratorijski kriterij u odsustvu kliničkog, postavlja se dijagnoza "vjerovatne APS".
11. Primjer: pacijent nije imao kliničke manifestacije APS u pozadini identificirane AFA. Koliko je opravdano imenovanje metipreda (deksametazon, prednizolon) takvom pacijentu kako bi se smanjio nivo antitela?
Trenutno medicina nema terapije koje smanjuju nivo antitela. Rezultati provedenih studija dokazuju da se glukokortikoidi, koji uključuju prednizolon, deksametazon i druge slične lijekove, ne bi trebali koristiti za liječenje APS-a, jer nemaju utjecaja na razinu AFA.
12. Koliko je opravdano imenovanje plazmafereze (x sesija) za smanjenje nivoa APA?
Uprkos činjenici da je plazmafereza sposobna mehanički ukloniti antitijela, ona, međutim, ni na koji način ne može spriječiti njihovu ponovnu sintezu. Ovaj postupak nema dokazanu efikasnost u liječenju APS-a, čak i više, može biti kompliciran raznim neželjenim pojavama. Međutim, treba imati na umu da se plazmafereza može propisati za neke pacijente s APS-om koji imaju komplikacije poput trombotičke trombocitopenične purpure.
13. Koliko je opravdano imenovanje heparina niske molekularne težine (fraksiparin, kleksan) na 3 sedmice pod kontrolom koagulograma za APS?
Treba odmah napomenuti da se heparini ili heparini niske molekularne težine propisuju sa odgovarajućim indikacijama za čitav period trudnoće, a ne na bilo koji način "tečajevima". Tokom takvog tretmana, nivo AFA se ne prati; nema potrebe za ponovljenim AFA testovima sa potvrđenim AFA. Što se tiče koagulograma, oni se izvode jednom u tromjesečju, češće samo kada se otkriju abnormalnosti u koagulogramima.
14. Koliko je opravdano imenovanje karantila u vezi sa APS-om?
Do sada medicini nisu poznati podaci o kontroliranim kliničkim ispitivanjima kurantila o njegovoj stvarnoj efikasnosti i sigurnosti kod trudnica s APS-om. Uprkos činjenici da su pozitivni učinci kurantila pronađeni u nekim studijama, potvrda ovih podataka potrebna je u odgovarajućim kliničkim ispitivanjima.
15. Koliko je opravdano imenovanje intravenskog imunoglobulina (IVIG) za APS?
U toku prethodnih studija dokazano je da je IVIG u slučaju trudnica sa APS manje efikasan od heparina. Uzimajući to u obzir, IVIG se trenutno ne preporučuje trudnicama s APS-om.
16. Koliko je opravdano imenovanje aspirina od 100 mg dnevno za APS praćeno koagulogramskom kontrolom?
S obzirom na činjenicu da je aspirin antitrombocitni lijek i nema značajniji utjecaj na pokazatelje koagulograma, možemo reći da nema potrebe za kontrolom koagulograma prilikom uzimanja ovog sredstva.
Dokazano je da u odsustvu liječenja, nivo AFA tokom trudnoće spontano fluktuira. A ako uzmemo u obzir činjenicu da se pad nivoa AFA ne može smatrati povoljnim prognostičkim znakom, onda možemo doći do zaključka da praćenje AFA tokom trudnoće jednostavno nema smisla. Takođe treba naglasiti da je terapija tokom trudnoće konstantna i ne smije ovisiti o nivou AFA.
18. Koliko je opravdano liječenje aspirinom i heparinom kada se otkrije AFA?
U svakom slučaju, specifičan izbor terapije treba napraviti samo uzimajući u obzir pojedinačne faktore u svakom slučaju. Istovremeno, postoje neke opšte preporuke za upravljanje trudnicama sa APS:
pacijentima s APS-om i prethodnom trombozom treba propisati antikoagulaciju s varfarinom uz održavanje INR na 2,0-3,0. Međutim, moramo imati na umu da je varfarin teratogeni lijek koji može dovesti do razvoja različitih deformacija u fetusu. Uzimajući to u obzir, vrijedi preporučiti, prije planiranja trudnoće, zamjenu varfarina nefrakcioniranim heparinom ili heparinom male molekularne težine, što se nastavlja tijekom cijele trudnoće. Varfarin se nastavlja nakon porođaja;
Pacijentima s APS-om i kasnim fetalnim gubitkom preporučuje se propisivanje kombinacije niskomolekularnog heparina i niskih doza (75-150 mg) aspirina tokom cijele trudnoće, a heparin se također propisuje 6-8 tjedana nakon porođaja;
Pacijentima s APS-om i preeklampsijom u anamnezi (eklampsija) preporučuje se propisivanje niskih doza aspirina, jer je učinkovito sredstvo za prevenciju eklampsije. Što se tiče heparina male molekularne težine, on bi trebao biti propisan na osnovu rezultata procjene krvotoka u posteljici;
Pacijentima sa AFA bez kliničkih znakova APS-a preporučuje se niska doza aspirina tokom cijele trudnoće. Što se tiče heparina niske molekularne težine, odluka o njihovoj primjeni donosi se pojedinačno i trenutno nije bilo adekvatnih kliničkih studija o ovom problemu. U slučaju da nema dodatnih čimbenika rizika, racionalno se ograničiti samo na imenovanje aspirina, međutim, u prisutnosti dodatnih čimbenika rizika za trombozu (na primjer, pušenje ili nasljedna trombofilija), može se razmotriti upotreba heparina.
Norme parametara koagulacije u trudnica
Kao što znate, parametri koagulograma za trudnice i ne-trudnice razlikuju se jedni od drugih. To je zbog izraženih promjena u pokazateljima hemostaze koje se javljaju u trudnoći.
Rezultati provedenih studija sugeriraju da normalnu trudnoću prati dvostruko povećanje sadržaja fibrinogena, kao i porast koncentracije brojnih faktora koagulacije za 200-1000%, poput VII, VIII, IX, X i XII. Uz to, tijekom trudnoće postoji značajan porast nivoa topivog kompleksa fibrina i D-dimera, a kod svake četvrte zdrave trudnice takav se porast može otkriti već u prvom tromjesečju.
Sve te promjene istovremeno se odvijaju u pozadini smanjenja prirodne antikoagulantne aktivnosti, što također može biti praćeno trostrukim smanjenjem nivoa proteina S.
Ako govorimo o definiciji "normi" tijekom trudnoće, tada rješenje ovog problema koči ne samo potreba za posebnim kliničkim studijama na zdravim trudnicama, već i vrlo velika individualna varijabilnost navedenih pokazatelja.
Tabela u nastavku prikazuje neke norme parametara koagulacije za normalnu trudnoću. Međutim, u svakom slučaju, ove norme treba smatrati samo indikativnim, jer su studije za njihovo određivanje provedene na relativno malom broju ispitanika. Čimbenici + 11-15 tjedana + 21-25 tjedana + 31-35 tjedana + 36-40 sedmica
Faktor VII +111 (60-206) +150 (80-280) +162 (84-312) +171 (87-336)
Faktor X +103 (62-169) +115 (74-177) +123 (78-194) +127 (72-208)
Faktor V +93 (46-188) + 82 (66-185) +82 (34-195) +85 (39-184)
Faktor II +125 (70-224) +125 (73-214) +115 (74-179) +115 (68-194)
Antifosfolipidni sindrom je autoimuna bolest koju karakterizira pojava antitela na fosfolipide, glavnu komponentu ćelijskih membrana. Antifosfolipidni sindrom i trudnoća usko su povezani, jedan je od vodećih faktora pobačaja. Njegov udio u tome je oko 30-35%. Među zdravim ljudima, antitela na fosfolipide nalaze se u 3-4%, a njihova visoka stopa je u 0,3% ispitanika.
Mlade žene su podložnije ovoj patologiji, učestalost pojave afs kod njih je 6-7 puta veća nego kod muškaraca. Takođe, ovaj sindrom se primjećuje kod djece.
Ovu je bolest prvi put 1986. godine opisao engleski naučnik Huhges.

Zašto nastaje?
Razlozi za razvoj APS-a još nisu precizno utvrđeni. Nejasno je zašto neki ljudi koji imaju visoke titre antifosfolipidnih antitela ne manifestiraju bolest? Brojni su faktori koji pokreću njegov razvoj. Uvjetno se mogu podijeliti na čimbenike koji uzrokuju primarnu i sekundarnu trombofiliju.
Primarna trombofilija inicira:
- hiperhomocisteinemija;
- sindrom nakupine trombocita
- mala količina antikoagulansa;
- velika količina i visoka aktivnost 8 faktora koagulacije;
- mala količina 11 i 12 faktora koagulacije krvi;
- fenomen polimorfizma u genu protrombina i u genu 5 faktora koagulacije.
Za sekundarnu trombofiliju, pokretački čimbenici bit će sljedeći:
- virusne i bakterijske infekcije (hepatitis A, B, C, mononukleoza, endokarditis koji je uzrokovan infekcijom);
- maligne novotvorine;
- lijekovi (hormoni, psihotropni lijekovi);
- genetska predispozicija (nošenje antigena određene prirode) i nasljednost (pojava bolesti kod osoba čiji su srodnici patili od nje);
- bolesti koje su autoimune prirode (squv, reumatoidni artritis, periarteritis nodosa);
- trauma;
- trudnoća i porođaj;
- mijeloproliferativne bolesti;
- antifosfolipidni sindrom;
- zatajenje srca sa simptomima stagnacije;
- upalni proces u crijevima;
- nefrotski sindrom.
Mehanizam bolesti
Osnova bolesti je tromboza arterija i vena neupalne geneze. Postoji dvofaktorska teorija koja iznosi APS kao faktor koji može izazvati trombozu. Ovaj faktor se ostvaruje u prisustvu okidača za trombofiliju.
Patogeneza antifosfolipidnog sindroma je u tome što se u telu bolesne osobe antitela na fosfolipide proizvode u određenoj količini. Potonji su bitna komponenta svih ćelija u ljudskom tijelu. Kao rezultat interakcije antitela i fosfolipida dolazi do kršenja regulacije homeostaze (konstantnosti u krvnom sistemu) prema hiperkoagulaciji. To se očituje činjenicom da trombociti stiču pojačano svojstvo adhezije (taloženja) i agregacije (lijepljenja).
Pored toga, mijenja se odnos između proizvodnje tromboksana i prostaciklina, koji su komponente sistema koagulacije krvi. Nivo antikoagulansa u krvi se takođe smanjuje, što dovodi do tromboze unutar žila. Tromboza postaje široko rasprostranjena; u trudnica pogađa placentni kompleks, što dovodi do pobačaja. U ranim fazama trudnoće poremećen je proces implantacije jajašca u matericu, a u kasnijim fazama dolazi do smanjenja i naknadnog prestanka fetalne ishrane kroz sistem placente.

Kliničke manifestacije antifosfolipidnog sindroma temelje se na generaliziranoj trombozi
Vrste antifosfolipidnog sindroma
Klasifikacija se temelji na principu porijekla i klinici. Postoje sljedeće vrste bolesti:
- primarni antifosfolipidni sindrom (ne postoji veza sa drugom patologijom koja bi ga mogla pokrenuti);
- sekundarni (javlja se zajedno sa drugom bolešću);
- katastrofalna (javlja se u obliku munjevite koagulopatije s pojavom multiple tromboze);
- AFL-negativni tip bolesti (markeri bolesti nisu pronađeni u analizi, ali postoje klinički znaci);
- APS sa manifestacijom sličnom lupusu.
Klinička slika
Simptomi antifosfolipidnog sindroma su raznoliki, ali najčešće manifestacije će biti tromboza i patologija trudnoće.
Krvni ugrušci nastaju u velikom broju; mogu se pojaviti u posudama različitih veličina, od kapilara do velikih arterija i vena. Ova činjenica utječe na činjenicu da su pogođeni svi tjelesni sustavi: kardiovaskularni, nervni i mnogi drugi.

APS počinje sa debiranjem venske tromboze
To mogu biti površinske i duboko smještene vene donjih ekstremiteta, zahvaćene su posude mrežnjače i jetra. Istodobno, tromboza u venama je pojava mnogostruko češća nego u arterijskom krevetu.
Tromboze se manifestiraju u sljedećim patologijama:
- plućne embolije;
- buddy-Chiari i sindromi inferiorne šuplje vene;
- nadbubrežna insuficijencija.
Što se tiče manifestacija tromboze u arterijskom krevetu, moždani udar ishemijske prirode, ovdje prevladavaju prolazni ishemijski napadi.
Hipertenzija je čest simptom. Može se razviti zbog ishemije unutar bubrega, krvnih ugrušaka u njemu ili infarkta ovog organa. Ako se arterijska hipertenzija kombinira s livedo reticularisom, trombotičnom lezijom vaskularnog korita mozga, tada se broj takvih znakova naziva Sneddonov sindrom.
Neurološke lezije daju se osjetiti zbog neurosenzornog gubitka sluha, progresivne demencije, oštećenja vidnog živca, napadaja, mijelitisa, hiperkineze.
Srce je uvijek uključeno u proces tokom afs. Postoji infarkt miokarda, kardiomiopatija, koja je povezana s ishemijom. Često se pojavljuju valvularne patologije, može doći do suženja i insuficijencije različitih ventila, protiv kojih je moguća pojava srčane astme i teška insuficijencija. Mitralni zalistak je često zadebljan (u 80% pacijenata), a trikuspidalni zalistak je pogođen u 9% slučajeva. Takav fenomen kao valvularna vegetacija tipičniji je za primarne afs.
Simptomi bubrega bit će proteini u mokraći; u težim slučajevima nije isključen akutni otkaz ovih organa.
Gastrointestinalni trakt s antifosfolipidnim sindromom osjeća se povećanjem jetre, krvarenjem različite lokalizacije, trombozom mezenterijalnih sudova i infarktom slezine.
Pri postavljanju dijagnoze liječniku pomažu kliničke manifestacije bolesti na koži. Najkarakterističnija je livedo mreža. Riječ je o prorijeđenoj vaskularnoj mreži na koži koja postaje izražena na niskim temperaturama. Takođe, postoje višestruka krvarenja u noktu, eritem na tabanima i dlanovima, mogu biti trofični čirevi, pa čak i gangrena.

Livedo mesh kod pacijenta sa antifosfolipidnim sindromom
Kosti se također podvrgavaju uništavanju, a najčešća manifestacija mišićno-koštanog sistema je nekroza glave bedrene kosti.
Poremećaji u krvnom sustavu uvijek su kod antifosfolipidnog sindroma, to su trombocitopenični poremećaji, krvarenja.
Vrijedno je napomenuti da ljudi s ovom bolesti često doživljavaju smanjenje vidne oštrine do sljepila.

Karakteristike APS-a kod djece
O trudnoći
Antifosfolipidni sindrom i trudnoća prilično su teška kombinacija.
Ozbiljnost ove kombinacije objašnjava se činjenicom da se krvni ugrušci u ovom sindromu stvaraju u posudama posteljice, a poznato je da je odgovorna za ishranu djeteta. Kao rezultat toga, hranjive tvari se u njega ne dovode i pojavljuju se razne komplikacije. Najčešći su placentna insuficijencija, gestoza, abrupcija posteljice, smrt djeteta u majci. Prema statistikama, fetalna smrt se najčešće opaža u drugom i trećem tromjesečju.
Sumnja na afs javlja se ako žena ima istoriju mrtvorođenih, 1 i veći broj pobačaja u periodu dužem od 10 tjedana, 3 ili više pobačaja u ranoj fazi formiranja fetusa, smrt djeteta od rođenja do 28 dana života, kao rezultat komplikacija preranog porođaja ili gestoze. Takođe, ideju o prisustvu antifosfolpidnog sindroma potiču epizode tromboze kod žena mlađih od 45 godina i patologije iz različitih sistema s neobjašnjivim uzrokom. Pacijente sa ovim simptomima treba pregledati na AF.

Probir je obavezan za žene s utvrđenim antifosfolipidnim sindromom najmanje 2 puta prije planirane trudnoće
U akušerstvu pacijenti sa afs imaju posebno mjesto i trebaju stalni nadzor medicinskog osoblja.
Kako prepoznati?
Dijagnoza antifosfolipidnog sindroma temelji se na kliničkim podacima i laboratorijskim pregledima. Ali vrijedi znati da su simptomi vrlo zamagljeni, tako da ne možete bez testova.
Liječnik prije svega sakuplja anamnezu. Pacijent treba reći da li je bilo epizoda tromboze, patologije trudnoće, uključujući i bliske rođake.
U 2006. godini revidirani su kriterijumi za ovu bolest.
Postoje klinički i laboratorijski kriteriji.
Među kliničkim se razlikuju sljedeći znakovi:
- Najmanje 1 epizoda tromboze u bilo kojoj posudi. Mora se snimati instrumentalno, tj. koristeći Doppler pregled ili angiografiju. Također se mora izvršiti morfologija, prema čijim rezultatima upalni proces u vaskularnom zidu treba biti minimalan.
- Patološki nastavak trudnoće, naime 1 ili više situacija u kojima je fetus umro nakon 10 tjedana intrauterinog razvoja (treba zabilježiti pomoću instrumentalnog pregleda da je fetus imao normalne morfološke znakove).
- Jedan ili više slučajeva preranog porođaja u 34. sedmici zbog insuficijencije u sistemu majka-placenta, kao i eklampsije.
- Tri ili više iznenadnih pobačaja prije 10 tjedana intrauterinog razvoja, osim ako nisu isključeni drugi razlozi.
Laboratorijski kriteriji:
I takođe lupus antikoagulant. Norme imunoglobulina klase G do 25 E / ml i klase M do 30 E / ml. Ova analiza se podnosi dva puta. Ako se nakon prvog puta pokaže pozitivnim, tada je sljedeći test zakazan nakon 6 tjedana. Potreba za dvostrukim testom krvi objašnjava se činjenicom da ponekad potpuno zdrava osoba ima lažno pozitivan rezultat.

Specifična manifestacija ove bolesti je prisustvo srednjih ili visokih titra Ig M i Ig G antitela na kardiolipin u najmanje 2 test tečnosti u roku od 12 nedelja.
Povećanje vremena zgrušavanja krvi, prisustvo antitela na beta2-glikoprotein (najmanje dva puta u 12 nedelja) takođe je znak antifosfolipidnog sindroma. Jedan od kriterija za prisustvo bolesti je odsustvo drugih koagulopatija.
Dijagnoza se postavlja ako postoji barem jedan klinički i laboratorijski znak.
Ozbiljnost i kontrola propisanog liječenja pomoći će u procjeni dodatnih dijagnostičkih metoda, i to:
- opći test krvi (smanjeni broj trombocita);
- koagulogram (odrediti pokazatelje koagulabilnosti INR, protrombinsko vrijeme, nivo fibrinogena);
- krv na RW (opaža se lažno pozitivan rezultat);
- coombsova reakcija (ima pozitivnu reakciju);
- imunološki pregled krvi (utvrđuje se visok sadržaj reumatoidnog faktora, antinuklearnih antitela);
- biohemijski test krvi.
Važno je znati da se za trudnice koagulogram mora uzimati jednom u 14 dana, a nakon porođaja u 3 i 5 danu. Pored toga, podvrgavaju se ultrazvuku fetusa u dinamici, izvode CTG, nadgledaju cirkulaciju krvi u sistemu majka-placenta doplerskim pregledom.
Kako bi potvrdio prisustvo krvnih ugrušaka u različitim organima, liječnik propisuje ultrazvučno snimanje bubrega, vena i arterija mozga i vrata, donjih ekstremiteta i očiju. Kateterizacija srca i angiografski pregled koronarnog sistema takođe se koriste za utvrđivanje prisustva ateroskleroze.
CT i MRI se rade kako bi se napravila razlika između krvnog ugruška unutar srčane šupljine i miksoidne mase. Radioizotopska scintigrafija propisana je za ispitivanje pluća, otkrivanje trombotičnih elemenata u njima.
Valvularni defekti, koji su nastali pod uticajem antifosfolipidnog sindroma, utvrđuju se pomoću Echo-KG.
Liječenje
Tretman antifosfolipidnog sindroma usmjeren je na sprečavanje nastanka krvnih ugrušaka.
Od recepcija koje nisu za lijekove, pacijent treba slijediti preporuke liječnika:
- izbjegavajte biti u istom položaju duže vrijeme;
- umjerena fizička aktivnost;
- ne bavite se sportovima koji mogu dovesti do ozljeda;
- kod žena s dijagnozom afs oralna kontracepcija je kontraindicirana;
- prije zatrudnjenja, žena treba posjetiti ginekologa i proći skrining.
Nakon procjene težine bolesti, liječnik propisuje jedan lijek ili skupinu lijekova.
Ako govorimo o trudnici, takav pacijent treba uzimati antitrombocitna sredstva, glukokortikosteroide u malim dozama i imunoglobuline za cijelo razdoblje trudnoće. Također im se propisuje heparin u obliku injekcija.
Glavne grupe lijekova za liječenje afs su:
- indirektni antikoagulansi (varfarin);
- ravne linije (Heparin);
- antitrombocitna sredstva (Aspirin, Curantil, Pentoksifilin);
- aminoholini (plakinil).
Najučinkovitiji lijek je Warfarin, doziranje takvog lijeka nije lako odabrati, kontrolira se međunarodnim normaliziranim vremenom (INR). Najboljom vrijednosti za afs smatra se INR vrijednost od 2 do 3.
Međutim, dugotrajnom upotrebom varfarina mogu se razviti brojne komplikacije. U ovom slučaju, liječnik propisuje heparin male molekularne težine. Dobar je jer se zbog svojih svojstava može dugo koristiti bez nuspojava. Uz to, dovoljna je jedna injekcija dnevno, što je vrlo povoljno za pacijenta. Tokom trudnoće koristi se s uspjehom, jer ne prolazi kroz placentnu barijeru.
Aminoholinska sredstva koja se koriste za SLE također su vrlo pogodna za antifosfolipidnu patologiju. Imaju antitrombotički efekat.
Moderni i visoko efikasni lijekovi koji se prepisuju pacijentima sa sistemskim eritemskim lupusom u prisustvu katastrofalne varijante AFS dokazali su se i aktivno se prepisuju (Retuximab).
Kao simptomatski tretman hipertenzije, inhibitori faktora konverzije angiotenzina su odabrani lijekovi.
Ako je sindrom poprimio teški tok, tada se koriste visoke doze glukokortikosteroida i antikoagulansa. Ponekad su naznačene plazmafereza (pročišćavanje krvne plazme) i transfuzija svježe smrznute plazme.

Ženama u položaju propisani su preparati gvožđa, folna kiselina, vitaminski kompleksi
Šta očekivati \u200b\u200bod ovog sindroma?
Sa modernim nivoom medicine moguće je nadati se dobrom ishodu trudnoće i porođaja. Uz pomoć brojnih lijekova moguće je kontrolirati bolest, naime minimizirati trombozu. Ako govorimo o sekundarnim afs, tada je važno izliječiti bolest koja ga je pokrenula.
Što se tiče prognoze, uzimaju se u obzir teško kombinovani antifosfolipidni sindrom i SLE (sistemski eritemski lupus), porast antitela na kardiolipin i hipertenzija.
Pacijenti sa ovim sindromom se prijavljuju kod reumatologa. Prikazana im je redovna isporuka koagulograma i serološki pokazatelji.
Zaključak
Antifosfolipidni sindrom je ozbiljna patologija. Preventivne mjere će biti pregled prije rađanja djece.
Među razlozima uobičajenog pobačaja trudnoće, poseban značaj daje se utjecaju stvaranja antitijela (autoimune reakcije) na neke vlastite fosfolipide na procese implantacije, rasta, razvoja embrija i fetusa, tijeka trudnoće i ishoda porođaja.
Pojam "Antifosfolipidni sindrom" (APS) označava skupinu autoimunih poremećaja koje karakterizira značajna količina antitijela na fosfolipide sadržane u krvnoj plazmi (antifosfolipidna antitijela), kao i na glikoproteine \u200b\u200bpovezane s tim fosfolipidima (β2-glikoprotein-I, aneksin V i / ili protrombin).
APS se javlja u do 5% slučajeva. Među pacijentima s ponovljenim pobačajem, učestalost ove patologije raste na 27-42%. Relevantnost APS leži u činjenici da je glavna komplikacija ove patologije tromboza. Rizik od trombotičkih komplikacija tokom trudnoće i u postpartalnom periodu značajno se povećava.
Faktori rizika
Jedan od faktora nastanka APS-a je genetska predispozicija za ovu patologiju. Tako se kod pacijenata sa APS antigeni HLA sistema nalaze češće nego u populaciji. Poznati su i porodični slučajevi APS, koji čine do 2% slučajeva. Drugi važan faktor je prisustvo bakterijske i / ili virusne infekcije, što ne isključuje mogućnost razvoja trombotičkih komplikacija u okviru APS-a.
Za provođenje patološkog procesa neophodno je prisustvo u tijelu ne samo antitijela na fosfolipide, već i takozvanih kofaktora, nakon vezivanja s kojima nastaju istinski kompleksi antigen-antitijelo. Kao rezultat djelovanja različitih faktora vanjskog i unutarnjeg okruženja (virusna infekcija, maligne novotvorine, djelovanje lijekova), AFA stupa u interakciju s kofaktorima, što dovodi do ozbiljnih poremećaja u sistemu koagulacije krvi. Istovremeno, prije svega, poremećeni su procesi mikrocirkulacije i događaju se promjene na vaskularnom zidu.
S obzirom na to da je antifosfolipidni sindrom jedna od najčešćih vrsta patologije sistema koagulacije krvi, njegovo prepoznavanje treba uključiti u dijagnostički postupak u svim slučajevima rane i, posebno, ponovljene venske i arterijske tromboze, tromboembolije, dinamičkih poremećaja cerebralne cirkulacije i ishemijskih moždanih udara , uključujući one koje se javljaju kod migrenskih sindroma, oštećenja pamćenja, pareza, oštećenja vida i drugih manifestacija, kao i kod trajnih pobačaja (intrauterina fetalna smrt, pobačaji).
Vrste antifosfolipidnog sindroma
Postoje primarni i sekundarni API-ji. Prisustvo sekundarnog APS-a je zbog autoimunih bolesti (sa sistemskim eritematoznim lupusom, periarteritis nodosa, itd.), Karcinoma, zaraznih bolesti, kao i izloženosti brojnim lekovima i toksičnim supstancama. Shodno tome, navedene bolesti i stanja su odsutna u slučaju primarnog APS-a.
U nekim slučajevima izolira se takozvani katastrofalni APS, koji karakterizira iznenadna i brzo razvijajuća se višestruka organska insuficijencija, najčešće kao odgovor na faktore kao što su zarazne bolesti ili operacija. Katastrofalni APS se manifestuje sindromom akutnog respiratornog distresa, oštećenom cerebralnom i koronarnom cirkulacijom, omamljenošću, dezorijentacijom, mogućim razvojem akutne bubrežne i nadbubrežne insuficijencije, trombozom velikih žila.
Simptomi i komplikacije bolesti
Ponavljajuća se tromboza jedna je od glavnih i najopasnijih kliničkih manifestacija APS-a. Najčešće se javlja venska tromboza, lokalizirana u dubokim venama nogu, što je povezano s rizikom od tromboembolije grana plućne arterije. Međutim, česti su slučajevi tromboze bubrežnih i jetrenih vena. Mogu se javiti trombotske lezije portala, subklavije, donje šuplje vene, cerebralnih žila, arterija i vena mrežnjače, velikih žila donjih ekstremiteta i različitih dijelova aorte. Kliničke manifestacije arterijske tromboze su periferna gangrena, sindrom aortnog luka, sljepoća, cerebrovaskularne nesreće itd. Rizik od trombotičkih komplikacija povećava se tokom trudnoće i u postpartalnom periodu.
Poznato je da APS dovodi do trudnoće koja nije u razvoju, intrauterinog zaostajanja u razvoju, sve do njegove smrti u II i III tromjesečju. U prvom tromjesečju trudnoće, AFA može imati direktan štetni učinak na jajnu stanicu s naknadnim spontanim pobačajem.
Od ranih faza trudnoće, bilježi se porast funkcionalne aktivnosti trombocita, smanjuju se sintetizirajuće proteine \u200b\u200bi hormonske funkcije posteljice. U nedostatku odgovarajućeg tretmana, dodaje se povećanje aktivnosti sistema koagulacije krvi. U tom slučaju dolazi do tromboze u posudama posteljice, razvija se placentna insuficijencija, hronična hipoksija i često fetalna smrt zbog nedostatka kisika.
Dijagnostika i liječenje
Za efikasnu dijagnozu APS sindroma čini se važnom sveobuhvatna procjena anamnestičkih, kliničkih i laboratorijskih podataka, što omogućava ispravnu procjenu rizika od komplikacija i pravovremenu propisivanje potrebne terapije. Prilikom vođenja trudnica i žena nakon porođaja koje pate od APS-a neophodno je pažljivo praćenje aktivnosti autoimunog procesa, stanja sistema koagulacije krvi, prevencije, dijagnoze i liječenja novih poremećaja.
Klinički kriteriji za dijagnozu APS su indikacije epizoda venske i arterijske tromboze, potvrđene laboratorijskim ili instrumentalnim studijama. Važni su i podaci o patološkom toku prethodnih trudnoća: spontani pobačaji prije 10 tjedana trudnoće iz neobjašnjivih razloga, kada smrt embrija (fetusa) zbog genetskih uzroka nije vjerovatna; fetalna smrt u roku od 10 tjedana, prerano rođenje, u pozadini teške gestoze i placentne insuficijencije.
Laboratorijski kriteriji za antifosfolipidni sindrom:
- Prisustvo antikardiolipinskih antitela klase IgG ili IgM u krvi u proseku ili u visokom titru u intervalu od 6 nedelja.
- Otkrivanje antikoagulansa lupusa (VA) u krvnoj plazmi u intervalu od 6-8 sedmica uz najmanje dvostruko povećanje.
Moguće je pretpostaviti razvoj APS-a u prisutnosti autoimunih bolesti, uobičajenog pobačaja (koji nije povezan sa endokrinim, genetskim uzrocima, abnormalnostima genitalnih organa, organske ili funkcionalne isthmic-cervikalne insuficijencije), s ranim razvojem preeklampsije, posebno njenih teških oblika, placentne insuficijencije, fetalne pothranjenosti tokom prethodnih trudnoća, lažno pozitivne Wassermanove reakcije.
Da bi se suzbio autoimuni proces, poželjno je propisati terapiju glukokortikoidima kao pripremu za trudnoću. Male doze prednizolona (5 mg) ili metipreda (4 mg dnevno) mogu smanjiti aktivnost autoimunog procesa i spriječiti razvoj poremećaja sistema koagulacije krvi. Terapiju steroidima treba provoditi tokom cijele trudnoće i u roku od 10-15 dana nakon porođaja, nakon čega slijedi postupno ukidanje. Da bi se spriječila reaktivacija virusne infekcije tijekom uzimanja glukokortikoida kod pacijenata sa APS, vrši se intravenozno kapanje imunoglobulina u dozi od 25 ml svaki drugi dan (3 doze). Uvođenje tako malih doza imunoglobulina poželjno je u prvom tromjesečju trudnoće, u 24. tjednu i prije porođaja.
Posebna pažnja posvećuje se korekciji poremećaja u sistemu koagulacije krvi. Kada se trombociti aktiviraju, propisani su antitrombocitni agensi: kurantil (75-150 mg dnevno), trental (300-600 mg) ili teonikol (0,045 mg dnevno). Nadzor sistema zgrušavanja krvi treba provoditi jednom u 2 sedmice. U slučajevima kada se patološka aktivnost trombocita kombinuje s povećanjem aktivnosti u vezi plazme i pojavom znakova intravaskularne koagulacije, opravdana je upotreba niskih doza heparina (5000 IU 2-3 puta dnevno supkutano). Trajanje terapije heparinom određuje se težinom poremećaja hemostaze. Upotreba malih doza aspirina (80-100 mg dnevno) pomaže pojačavanju djelovanja heparina. Heparini niske molekularne težine široko se koriste za liječenje APS-a. Upotreba ovih lijekova u malim dozama ne zahtijeva strogo praćenje stanja sistema koagulacije krvi kao kada se koristi konvencionalni heparin.
Plazmafereza se koristi kao dodatna metoda liječenja APS-om. Primjena ove metode omogućava normalizaciju reoloških svojstava krvi, smanjenje prekomjerne aktivacije sistema koagulacije krvi, smanjenje doze kortikosteroidnih lijekova i heparina, što je posebno važno u slučaju loše podnošljivosti. Glavni terapijski efekti plazmafereze uključuju: detoksikaciju, korekciju reoloških svojstava krvi, imunokorekcija, povećana osjetljivost na endogene supstance i lijekove. Uklanjanje antifosfolipidnih autoantitela, imunih kompleksa, imunogenih proteina plazme i autoantigena tokom postupka od posebnog je značaja u lečenju pacijenata sa APS, što omogućava smanjenje aktivnosti autoimunog procesa. Plazmafereza se može koristiti i kao priprema za trudnoću i tokom nje i učinkovita je metoda liječenja pacijenata s APS-om.
Pregled i priprema lijekova za pacijente sa APS trebaju započeti prije trudnoće. U isto vrijeme, pritužbe i anamneza pacijenta pažljivo se analiziraju kako bi se identificirali mogući znakovi bolesti. Laboratorijski testovi se izvode kako bi se otkrila antitela na kardiolipin i lupus antikoagulant. Ako su identificirani, studija se ponavlja nakon 6-8 tjedana. Istovremeno se vrši pregled radi utvrđivanja popratnih bolesti i, ako je potrebno, njihovog liječenja. U prisustvu ponovljenih pozitivnih testova na prisustvo antitela na kardiolipin i lupus antikoagulant, tretman APS-om započinje individualnim odabirom lekova.
Na početku trudnoće, u ranim fazama, prirodu toka bolesti prati se odgovarajućim laboratorijskim testovima i provodi se potrebno liječenje. Uz pomoć ultrazvuka prate se stope rasta fetusa u razmaku od 3-4 tjedna i procjenjuje se funkcionalno stanje fetoplacentarnog sistema. Dopler ultrazvuk je od posebne dijagnostičke vrijednosti koji se izvodi od 20 tjedana s razmakom od 3-4 tjedna prije porođaja. Doppler analiza omogućava pravovremenu dijagnozu smanjenja fetoplacentalnog i uteroplacentarnog krvotoka i omogućava procjenu efikasnosti terapije. Podaci kardiotokografije nakon 32. gestacijske sedmice također nam omogućuju procjenu funkcionalnog stanja fetusa. Tokom porođaja provodi se pažljiv nadzor srca u vezi sa prisutnošću hronične fetalne hipoksije, kao i povećanim rizikom od abrupcije normalno smještene posteljice, razvojem akutne fetalne hipoksije u pozadini hronične. Preporučljivo je utvrditi stanje sistema koagulacije krvi neposredno prije porođaja i tokom porođaja.
Od posebnog je značaja promatranje stanja puerpera, jer se u postpartalnom periodu povećava rizik od tromboembolijskih komplikacija. Terapija steroidima nastavlja se 2 sedmice s postupnim povlačenjem. Poželjno je nadgledati sistem hemostaze 3. i 5. dan nakon porođaja. Uz ozbiljnu hiperkoagulaciju, potreban je potkožni kratki kurs heparina, 10.000-15.000 jedinica dnevno. Pacijenti kojima su propisani antikoagulanti i antitrombociti potiskuju laktaciju. Pacijente kojima je dijagnosticiran APS tokom trudnoće treba pažljivo pratiti i nadgledati stanje sistema koagulacije krvi zbog rizika od napredovanja bolesti.
Dakle, pravovremena dijagnoza, priprema i racionalno vođenje trudnoće kod pacijenata sa APS uz upotrebu adekvatnog tretmana smanjuje rizik od komplikacija tokom trudnoće i u postpartalnom periodu.
Antifosfolipidni sindrom je najčešći uzrok trombofilnih komplikacija i pratećeg uobičajenog gubitka trudnoće. Razlikovati primarni antifosfolipidni sindrom od sekundarnog - u prisustvu autoimune bolesti (najčešće je to sistemski eritemski lupus). Nema velike razlike u svim parametrima između primarnog antifosfolipidnog sindroma i sekundarnog, samo se simptomi autoimune bolesti dodaju sekundarnom. Postoji i "katastrofalni antifosfolipidni sindrom".
Uzrok antifosfolipidnog sindroma ostaje nejasan, vjeruje se da virusne infekcije igraju ulogu. Patogeneza antifosfolipidnog sindroma povezana je sa činjenicom da su autoantitela sa heterogenom specifičnošću usmerena protiv negativno nabijenih fosfolipida ili proteina koji vežu fosfolipid.
Na osnovu brojnih studija radne grupe stručnjaka iz ove oblasti, na posljednjem simpozijumu u septembru 2000. godine u Francuskoj, usvojeni su sljedeći kriterijumi za antifosfolipidni sindrom, tako da se mogu usporediti studije provedene u različitim zemljama.
Kriteriji za klasifikaciju i definiciju API-ja
Klinički kriteriji
Vaskularna tromboza - jedna ili više kliničkih epizoda arterijske, venske u bilo kojem tkivu ili organu. Trombozu treba potvrditi Doppler-om ili histološkim pregledom, osim površinske tromboze malih vena. Za histološku potvrdu, tromboza ne bi trebala biti praćena upalnim procesima u vaskularnom zidu.
Tokom trudnoće:
- Jedna ili više nejasnih smrtnih slučajeva morfološki normalnog fetusa starijeg od 10 tjedana trudnoće, s normalnom morfologijom ultrazvukom ili direktnim ispitivanjem fetusa.
- Jedno ili više prijevremeno rođenih morfološki normalnih novorođenčadi prije 34. tjedna gestacije zbog preeklampsije ili eklampsije ili teške placentne insuficijencije.
- Tri ili više nejasnih uzroka spontanih pobačaja prije deset tjedana trudnoće kod majke nakon isključivanja anatomskih, hormonalnih i genetskih uzroka pobačaja.
Laboratorijski kriteriji:
- Anti-kardiolipinska antitijela na IgG i / ili IgM izotipe u krvi, sa prosječnim ili visokim titrom 2 ili više puta zaredom u studiji s razmakom od 6 tjedana, proučavanoj standardnim imunoasorbentnim testom vezanim za enzim za antikardiolipinska antitijela beta-glikoprotein-1-zavisna.
- Lupus antikoagulant prisutan u plazmi 2 ili više puta zaredom, testiran u intervalima od 6 tjedana, testiran prema smjernicama Međunarodnog društva za trombozu i hemostazu na sljedeći način:
- Produljenje koagulacije zavisne od fosfolipida u koagulacijskim testovima: aktivirano parcijalno tromboplastinsko vrijeme (APTT); vrijeme zgrušavanja kod koze; istraživanje zmijskog otrova; produženje protrombinskog vremena, textarin-time.
- Neprilagođavanje vremena zgrušavanja u skrining testu u kombinaciji sa normalnom plazmom osiromašenom trombocitima.
- Skraćivanje ili ispravljanje produženog vremena koagulacije dodavanjem viška fosfolipida u skrining test.
- Isključenje drugih koagulopatija, tj. inhibitor faktora VIII, heparin itd.
Laboratorijski kriteriji isključili su takve testove kao što su niske razine antikardiolipinskih antitijela, IgA-antikardiolipinska antitijela, anti-beta2-glikoprotein-1, antitijela na protrombin, aneksin ili neutralni fosfolipidi, lažno pozitivna Wassermanova reakcija.
Radna grupa vjeruje da ove metode zahtijevaju daljnje proučavanje. Što se tiče anti-beta2-glikoproteina-1, koji, prema većini istraživača, igra ključnu ulogu u pojavi trombofilije, ovom testu je potrebna unutarlaboratorijska standardizacija i tehničko poboljšanje. Možda će u budućnosti ovaj test biti glavni kriterij u dijagnozi antifosfolipidnog sindroma.
Trenutno postoje studije o ulozi anti-beta2-glikoprotein-1 IgA i IgG u razvoju antifosfolipidnog sindroma. U grupama žena sa kliničkom slikom antifosfolipidnog sindroma u odsustvu kardiolipinskih antitela i VA otkriven je visok nivo ovih antitela.
Prema literaturi, učestalost antifosfolipidnog sindroma među pacijentima s uobičajenim gubitkom trudnoće iznosi 27-42%.
Učestalost naseljenosti ovog stanja kod nas nije proučavana, au SAD iznosi 5%.
Postoje dvije klase antifosfolipidnih antitela nastalih pod uticajem endogenih podražaja:
- Antifosfolipidna antitela koja produžuju in vitro reakcije koagulacije zavisne od fosfolipida dejstvom na Ca 2+ - zavisno vezivanje protrombina i faktora Xa, Va tokom sklapanja kompleksa protrombin-aktivatora (protrombinaza) - lupus antikoagulant (VA);
- Antifosfolipidna antitela koja se određuju imunološkim testovima na osnovu kardiolipin - antikardiolipinskih antitela (AKA).
Autoantitela na fosfolipide mogu nastati pod uticajem egzogenih i endogenih stimulusa. Egzogeni podražaji povezani su uglavnom sa zaraznim antigenima, dovode do stvaranja prolaznih antitijela koja ne uzrokuju tromboembolijske poremećaje. Primjer takvih egzogenih antifosfolipidnih antitijela su antitijela otkrivena Wassermanovom reakcijom.
Antitela nastala pod uticajem endogenih podražaja povezana su sa oštećenom endotelnom hemostazom. Ova antifosfolipidna antitijela uzrokuju tromboembolijske poremećaje, često povezane s moždanim udarima, srčanim napadima kod mladih, s drugim trombozama i tromboembolijom i razvojem Snedonovog sindroma. Objašnjenje ovog fenomena dobiveno je posljednjih godina, kada je utvrđeno da je za vezivanje antitijela prisutnih u serumima pacijenata sa autoimunim, ali ne i zaraznim bolestima, kardiolipinom neophodno prisustvo komponente plazme (kofaktora) koja je identificirana kao beta-glikoprotein-1 beta1- GP-1). U detaljnijoj studiji ovog fenomena naučnici su pokazali da antitela na kardiolipin izolovana iz seruma bolesnika sa autoimunim bolestima reaguju sa kardiolipinom samo u prisustvu uGP-1, dok se vezivanje antitela na kardiolipin (ACA) sintetiše kod pacijenata sa različitim zaraznim bolestima ( malarija, infektivna mononukleoza, tuberkuloza, hepatitis A i sifilis) nisu zahtijevali kofaktor u sistemu. Štaviše, dodavanje beta2-GP-1 u nekim je slučajevima inhibiralo interakciju seruma kod pacijenata sa zaraznim bolestima sa kardiolipinom. Klinička analiza dobivenih rezultata pokazala je da je razvoj trombotičkih komplikacija povezan sa sintezom kofaktor-ovisnih antitijela na kardiolipin. Međutim, prema drugim podacima, čak i kod pacijenata sa antifosfolipidnim sindromom, uprkos prisustvu beta2-GP-1, sposobnost antitela na fosfolipide (APA) da interaguju sa kardiolipinom određena je nizom drugih faktora. Dakle, vezivanje niskoavidnih antifosfolipidnih antitela za kardiolipin u većoj mjeri ovisi o prisutnosti kofaktora u sustavu nego što je potrebno u slučaju prisustva visokoavidnih antitijela u serumima pacijenata. Suprotno tome, A.E. Gharavi (1992) naglašava da je ovisnost o kofaktorima karakteristična za vrlo strasna antitijela. Ranije je u proučavanju seruma bolesnika s antifosfolipidnim sindromom pokazano da se u njihovom krvnom serumu, pored antifosfolipidnih antitela, nalazi i veliki broj različitih proteina koji vežu fosfolipide koji reaguju sa anionskim fosfolipidima (apolipoproteini, lipokortini, placentni antikoagulacijski proteini, koagulacioni protein, koagulacioni protein). proteini itd.).
Gornji podaci sugeriraju prisustvo najmanje dvije populacije antitela koja vežu kardiolipin. Neka od njih ("zarazna" antitijela) imaju sposobnost da direktno prepoznaju negativno nabijene epitope fosfolipida, dok druga ("autoimuna" antitela) reaguju sa složenim epitopom koji se sastoji od fosfolipida i beta2-HP-1, a možda i drugih proteina koji vežu fosfolipid.
Razvoj trombotičkih komplikacija povezan je sa sintezom "autoimunih" (zavisnih od kofaktora) antitela.
U akušerskoj praksi lupus antikoagulant je od velike važnosti. Smatra se da je otkrivanje antikoagulansa lupusa u krvi kvalitativna manifestacija učinka određenih nivoa autoantitela na fosfolipide (kardiolipin, fosfatidiletanol, fosfatidilholin, fosfatidilserin, fosfatidilinazitol, fosfotidilna kiselina) na stanje hemostaze.
Izuzetno zanimljiv pristup tumačenju imunoloških aspekata pobačaja predstavljen je u radovima A. Beer i J. Kwak (1999, 2000). Autori razlikuju 5 kategorija imunoloških poremećaja koji uzrokuju ponovljeni pobačaj, neuspjehe IVF-a i neke oblike neplodnosti.
- Kategorija I - kompatibilnost supružnika prema HLA sistemu i odnos trenutno poznatih antigena HLA sistema sa oštećenom reproduktivnom funkcijom. Prema autorima, kompatibilnost s HLA dovodi do neefikasne "kamuflaže" placente i čini je dostupnom za majčin imunološki napad.
- II kategorija - antifosfolipidni sindrom povezan sa cirkulacijom antifosfolipidnih antitela. Incidencija antifosfolipidnog sindroma kod pacijenata sa ponovljenim pobačajem je 27-42%. Patogenetska osnova neuspješnog završetka trudnoće kod APS-a su trombotske komplikacije nastale na nivou uteroplacentarnog bazena. Pored toga, fosfotidilserin i fosfotidiletanalamin igraju važnu ulogu u procesu implantacije kao "molekularni ljepilo". U prisustvu antitela na ove fosfolipide, diferencijacija citotrofoblasta u sincitiotrofoblasti može biti poremećena, što dovodi do smrti trudnoće u ranim fazama.
- III kategorija imunoloških poremećaja uključuje antinuklearna, antihistonska antitela, koja čine 22% pobačaja imunološke geneze. U prisustvu ovih antitela možda neće biti manifestacija autoimunih bolesti, ali u posteljici se nalaze upalne promene.
- IV kategorija - prisustvo antispermijskih antitela. Ova kategorija imunoloških poremećaja javlja se u 10% pacijenata sa ponovljenim pobačajem i neplodnošću. Antispermna antitela se otkrivaju kada žene imaju antifosfolipidna antitela na serin ili etanolamin.
- Kategorija V je najozbiljnija, uključuje 45% žena s neuspjehom IVF-a s poremećajima implantacije. U ovoj kategoriji postoji nekoliko odjeljaka.
Odjeljak 1 povezan je s povećanjem sadržaja prirodnih ćelija ubojica CD 56 u krvi za preko 12%. Prema autorima, s porastom CD 56+ iznad 18%, smrt embrija se uvijek dogodi. Ova vrsta ćelija se otkriva i u krvi i u endometriju. Pored svoje citotoksične funkcije, sintetišu proupalne citokine, uključujući TNFa. Kao rezultat viška proupalnih citokina, poremećeni su procesi implantacije, oštećene ćelije trofoblasta, praćene razvojem insuficijencije trofoblasta i placente i smrću embrija / fetusa (slični podaci dobiveni su od drugih autora).
Drugi odjeljak V kategorije povezan je s aktivacijom CD19 + 5 + ćelija. Nivo preko 10% smatra se patološkim. Glavni značaj ovih ćelija povezan je s proizvodnjom antitela na hormone koji su neophodni za normalan razvoj trudnoće: estradiol, progesteron, horionski gonadotropin. Pored toga, moguća je pojava antitela na hormone štitnjače, hormone rasta. Patološka aktivacija CD 19 + 5 + razvija neuspjeh lutealne faze, neadekvatan odgovor na stimulaciju ovulacije, sindrom "otpornih jajnika", prerano "starenje" jajnika i prevremenu menopauzu. Pored izravnog učinka na navedene hormone, kod prekomjerne aktivnosti ovih ćelija nedostaju pripremne reakcije za implantaciju u endometrijumu i u miometriju, a kasnije i u decidualno tkivo. To se izražava u upalnim i nekrotičnim procesima u decidui, kršenjem stvaranja fibrinoida, u prekomjernom taloženju fibrina.
Odeljak 3 se bavi visokim nivoom CD 19 + 5 + ćelija, koje proizvode antitela na neurotransmitere, uključujući serotonin, endorfine i enkefaline. Ta antitijela doprinose otpornosti jajnika na stimulaciju, utječu na razvoj miometrija i doprinose smanjenju cirkulacije krvi u maternici tijekom implantacije. U prisustvu ovih antitijela, pacijenti mogu imati depresiju, fibromialgiju, poremećaj spavanja i paniku.
Takav diferencirani pristup omogućava individualni pristup rješavanju pitanja uloge različitih imunoloških aspekata u nastanku uobičajenog gubitka trudnoće. Nažalost, tako jasna podjela u kliničkoj praksi ne djeluje. Najčešće pacijenti sa antifosfolipidnim sindromom mogu imati antitela na hCG i antitiroidna antitela, itd.
Posljednjih godina vrlo se široko raspravlja o problemu aloimunih odnosa u pogledu kompatibilnosti antigena HLA sistema. Mnogi istraživači dovode u pitanje postojanje ovog problema, s obzirom na to da HLA antigeni nisu eksprimirani na trofoblastu. Istraživanja o ovom pitanju pokrenuta su još 70-ih godina. Brojni istraživači vjerovali su da senzibilizaciju leukocita, poput senzibilizacije eritrocita, prati spontani pobačaj. U Rh i ABO trudnoći, najčešća komplikacija trudnoće je prijetnja prekidom. Ali čak i bez senzibilizacije, prijetnja prekidom je njegova najčešća komplikacija. Čak i uz ozbiljna oštećenja fetusa i njegovu smrt zbog hemolitičke bolesti, abortus se često ne dogodi spontano. Rad koji smo obavljali niz godina pokazao je da uobičajeni pobačaj u pravilu nema direktne etiološke veze sa senzibilizacijom za Rh i ABO. Česti prekidi, posebno nakon 7-8 tjedana (vrijeme kada se Rh faktor pojavljuje u fetusu), mogu dovesti do senzibilizacije, što komplikuje tok trudnoće. Teški problemi nastaju u vođenju ove trudnoće. Isplati li se ispitivati \u200b\u200bi liječiti uobičajeni pobačaj ako pacijent ima Rh senzibilizaciju, jer zadržavanjem trudnoće u ranim fazama možete kasnije dobiti fetus s edematoznim oblikom hemolitičke bolesti?
U literaturi se posebna pažnja posvećuje ulozi antigena histokompatibilnosti u pobačaju. Vjerovatnoća majčine alosenzibilizacije za fetalne antigene leukocita je prilično velika, s obzirom na njihovo rano stvaranje i sposobnost prolaska kroz placentu. Pitanje etiološke uloge senzibilizacije leukocita smatra se krajnje kontroverznim. Mnogi istraživači etiološki povezuju leukosenzibilizaciju sa pobačajem i preporučuju imunosupresivnu terapiju.
Analiza podataka pokazala je da se kod zdravih višerodnih žena senzibilizacija na antileukocite opaža mnogo češće nego kod trudnica s ponovljenim pobačajem (33,6%, odnosno 14,9%). Istodobno se otkrivaju brojne osobine: kod žena koje su imale višestruku trudnoću koja je završila normalnim porođajem, leukosenzibilizacija je bila 4 puta vjerojatnija od one kod kojih je trudnoća prekinuta umjetnim pobačajem (odnosno 33,6% naspram 7,2%). Često otkrivanje ovih antitijela u krvi zdravih, višerodnih žena svjedočilo je o njihovoj neškodljivosti za procese reprodukcije. S druge strane, porast učestalosti pojave limfocitotoksičnih i leukoaglutinirajućih antitijela u krvi zdravih žena s povećanjem broja normalnih trudnoća završenih porođajem ukazuje na fiziološki, a ne na patološki značaj ove vrste izosenzibilizacije. Proizvodnja antitela protiv leukocita prirodni je proces, jer fetus nužno sadrži transplantacijske antigene koji su nespojivi s majkom, a čini se da štite fetus od štetnih efekata majčinih imunoloških limfocita.
Prema istraživačkim podacima, prilikom proučavanja pokazatelja staničnog imuniteta u trudnica sa pobačajem nije bilo moguće uočiti primjetne razlike kod njih u odnosu na žene u fiziološkoj trudnoći. Značaj reakcije blast transformacije s fitohemaglutininom, intenzitet reakcije blast transformacije u mješovitoj kulturi limfocita i sadržaj serumskih imunoglobulina nisu se statistički razlikovali. Istodobno, tijekom pobačaja, serum žena značajno je češće stimulirao stanični imunitet, a faktor seruma koji blokira otkriven je u nekompliciranoj trudnoći. Tokom fiziološkog toka trudnoće, senzibilizacija limfocita na fetalne antigene utvrđena je kod 83,3% žena. U trudnica sa ponovljenim pobačajem senzibilizacija ćelija bila je slabija i rjeđa; blokirajući učinak seruma obično je izostao.
Otkrivene razlike ukazuju na slabljenje blokirajućih svojstava seruma trudnica s prijetećim spontanim pobačajem. Izgleda da imunoregulacijska svojstva krvnog seruma igraju presudnu ulogu u razvoju trudnoće. Sa smanjenjem blokirajućih svojstava seruma, aktiviraju se mehanizmi koji dovode do pobačaja. Do sličnih podataka došli su mnogi istraživači.
Mnogi istraživači ne prihvaćaju ovu teoriju o ulozi svojstava blokiranja seruma u održavanju trudnoće. Njihova glavna motivacija je da postoje žene u normalnoj trudnoći koje nemaju blokirajuća antitijela.
Štaviše, metode za otkrivanje blokirajućih antitela nisu standardizovane i imaju malu osetljivost kako bi se tačno i u različitim laboratorijama dobili slični rezultati. Određivanje blokiranja antitijela reakcijom mješovite kulture limfocita također ima niz nedostataka:
- varijabilnost odgovora kod različitih pacijenata, pa čak i kod istih, ali izvedenih u različito vrijeme;
- poteškoće u procjeni stepena suzbijanja u odnosu na blokirajuću aktivnost;
- osetljivost metode je nepoznata;
- ne postoji standardizacija metode i standarda za procjenu rezultata;
- ne postoji jedinstvena metoda za tumačenje podataka.
Uprkos tome, mnoge istraživačke grupe ovaj problem razmatraju među imunološkim faktorima pobačaja. Smatra se da blokirajuća antitijela mogu djelovati na nekoliko načina. Mogu biti usmjereni protiv antigen-specifičnih receptora na majčinim limfocitima, što sprječava njihovu reakciju na antigene fetoplacentarnih tkiva; ili mogu reagirati s fetoplacentarnim tkivnim antigenima i blokirati njihovo prepoznavanje majčinim limfocitima. Također se vjeruje da su blokirajuća antitijela anti-idiotipska antitijela usmjerena protiv antigen-specifičnih strana (idiotipova) drugih antitijela, tj. antigeni-receptori na površini limfocita T mogu biti vezani i zbog toga spriječeni da djeluju na fetus. Postoje dokazi da mogu biti povezani sa anti-HLA-DR antigenima i sa receptorima anti-Fc antitijela.
Pored blokiranja antitijela, postoje i dokazi o ulozi limfocitoksičnih antitijela protiv muževih limfocita. Većina istraživača vjeruje da su ona, poput blokiranja antitijela, posljedica normalne trudnoće. U 20% ih se otkrije nakon prve normalne trudnoće, a ima ih u 64% mnogih žena koje rađaju sigurno. U žena s ponovljenim pobačajem, one su mnogo rjeđe (od 9 do 23%).
Uz to, postoje studije koje pokazuju da prisustvo neutrofilno specifičnih antitela kod majke protiv očevih antigena može biti praćeno ozbiljnom neutropenijom u fetusu. Neutrofil-specifične antigene NA1, NA2, NB1 i NC1 prvi su karakterizirali Lalezari i sur. (1960). Ostale neutrofilne antigene NB2, ND1, NE1 otkrili su Lalezari i sur. (1971), Verheugt F. i dr. (1978) Claas F. i dr. (1979).
N antigeni su nezavisni od drugih antigena prisutnih na površini neutrofila, poput HLA f. Najznačajniji antigeni koji uzrokuju proizvodnju antitela su antigeni NA 1 i NB1, a stopa otkrivanja antitela specifičnih za neutrofil varira u različitim studijama od 0,2% do 20%. Ova razlika nastaje zbog činjenice da su se tek nedavno pojavile metode za otkrivanje ovih antitela i zbog toga što je teška neutropenija kod novorođenčadi retka. Ta djeca najčešće rano zaraze i vrlo brzo pređu u sepsu. Stoga autori preporučuju da se kod novorođenčadi s nejasnom neutropenijom, posebno kod nedonoščadi, testira prisustvo antitela na neutrofile u majčinoj krvi. Kod majke prisustvo antitela na neutrofile ne daje neutropeniju, poput Rh antitela, pod uslovom da nisu autoimune.
Žene sa spontanim pobačajem mogu otkriti autoantitela protiv sopstvenih limfocita - limfocitotoksična autoantitela, koja se kod žena sa ponovljenim pobačajem otkrivaju u 20,5% slučajeva, dok tokom fiziološke trudnoće nisu otkrivena.
Smanjenje blokirajućih svojstava seruma povezano je s kompatibilnošću supružnika za antigene sistema HLA (humani lejkociteantigeni). HLA sistem ili stari naziv "glavni kompleks histokompatibilnosti" grupa je gena čiji proteini služe kao markeri identiteta na površini različitih ćelija, s kojima T-limfociti komuniciraju kroz vlastite receptore u imunološkom odgovoru. Prvi put su identificirani u reakciji odbacivanja grafta. HLA se sastoji od grupe gena klase I, II i III koji se nalaze na hromozomu 6. Ovaj sistem ima ogroman polimorfizam i samo unutar jednog hromozoma broj mogućih kombinacija njegovih gena je 3x10 6.
HLA klasa I uključuje lokuse HLA-A-B i -C - ovi geni predstavljaju porodicu peptida koji reaguju sa T-citotoksičnim (CD8 +) ćelijama.
Klasa II uključuje lokuse HU \\ DP, -DQ i DR - oni uglavnom komuniciraju s T-pomagačima (CD4 +). Genska klasa regije III uglavnom je uključena u upale, sadrži alele komponenata komplementa C2, C4 i Bf (Properdin faktor), kao i TNF (faktor nekroze tumora) i brojne izoenzime. Pored toga, nedavno je otkriveno da molekuli klase I također stupaju u interakciju s NK ćelijama kako bi spriječili lizu ćelija.
Velika grupa imunoglobulina, slična receptorima NK ćelija, nalazi se na hromozomu 19 - to su takozvani neklasični lokusi HLA-E, -F i G. Oni takođe učestvuju u imunološkim odgovorima, a fetalni HLA-G lokus se izražava na trofoblastu.
Alelne varijante gena imaju različite učestalosti pojavljivanja. Osobina frekvencije alela koristi se kao genetski marker za niz patoloških stanja.
Poslednjih godina vrlo se intenzivno proučava odnos HLA sistema sa različitim bolestima. Tako je utvrđeno da se autoimune bolesti poput artritisa, Reiterove bolesti opažaju kod 95% pacijenata sa alelom HLA B27, tj. gotovo 20 puta češće nego što se ovaj antigen nalazi u populaciji.
HLA DQ4 određuje se u 86,4% pacijenata sa antifosfolipidnim sindromom. Ako muž ima HLA DQ 201 - u 50% slučajeva će biti anembryonia.
Ako supružnik ima HLA B14, potrebno je ispitati prisustvo gena za adrenogenitalni sindrom; kod HLA B18 postoji velika vjerovatnoća da ćete imati dijete s razvojnim anomalijama.
Kod ponavljajućih pobačaja zabilježen je porast učestalosti pojave nekih alela i HLA fenotipova: A19, B8, B13, B15, B35, DR5, DR7, njihova učestalost je 19%, 9,5%, 19%, 17,5%, 22,2% , 69,6% i 39,1% naspram 6,3%, 3,8%, 10,3%, 16,7%, 29,9% i 22,7%, kod žena sa nekompliciranom trudnoćom.
Pored fenotipa HLA, mnogi istraživači vjeruju da kompatibilnost HLA antigena među supružnicima igra vrlo važnu ulogu. Glavna ideja je da se s HLA kompatibilnošću antitijela koja igraju ulogu faktora blokiranja ne razvijaju. Ako su supružnici kompatibilni s više od 2 HLA antigena, rizik od pobačaja je gotovo 100%.
Kompatibilnost supružnika prema HLA sistemu i njegov značaj u reprodukciji dugo su bili u polju imunologa i akušera. Postoji čitav niz istraživanja o ulozi limfocitoterapije u liječenju ponovljenih pobačaja korištenjem limfocita oca ili donatora, ili oboje. Mnogi su zagovornici ove terapije.
Istodobno, postoji mnogo protivnika ove terapije koji vjeruju da malo vjerovatno da će kompatibilnost igrati ulogu, a limfocitoterapija ne daje isti učinak kakav je postignut kod pristaša ove terapije.
Dobiveni su različiti rezultati iz metodički različitih pristupa rješavanju ovog problema: različite skupine pacijenata, različit broj ubrizganih limfocita, različiti periodi trudnoće u kojima se provodi terapija itd.
U literaturi postoji i originalno gledište o sistemu HLA prema Chiristiansen O.B. i dr. (1996), učinak kompatibilnosti roditeljskog antigena može biti neimunološkog porijekla. U eksperimentima na mišjim embrionima, autori su pokazali postojanje smrtonosnog recesivnog gena usko povezanog sa HLA. Mišji embriji homozigotni za određene alele HLA umiru u različitim fazama embriogeneze. HLA sličan kompleks se može naći i kod ljudi. Ako je to slučaj, roditeljska HLA kompatibilnost može biti sekundarna, što odražava homozigotnost za embrion za smrtni gen povezan sa HLA.