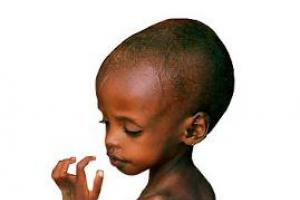
Não será segredo para ninguém que uma alimentação adequada é de grande importância na vida de cada pessoa. O mesmo se aplica às crianças. Neste artigo, gostaria de falar em detalhes sobre um problema como a desnutrição protéico-energética.
O que é isso?
No início, você precisa decidir sobre os conceitos que serão utilizados no artigo. O que é deficiência protéico-energética provavelmente é claro para todos. Isso é falta de proteínas no corpo da criança. Vale esclarecer também que esta condição é patológica. Mais precisamente, o corpo humano recebe pouca ou nenhuma proteína sob qualquer forma. Isto também pode ser causado pela decomposição muito rápida da substância. Nesse caso, a causa desse fenômeno pode ser queimaduras, doenças sépticas purulentas ou lesões graves.
Motivos principais
Por que pode ocorrer desnutrição protéico-energética? Vale dizer que esse problema é muito comum entre residentes de países em desenvolvimento. Durante os períodos de greve de fome, o percentual de pessoas com esta doença chega a 25%. Nesse caso, a causa é a quantidade insuficiente ou a baixa qualidade dos alimentos. O problema é agravado pela falta de fornecimento de energia. E tudo porque os aminoácidos dos alimentos, neste caso, não são utilizados na alimentação, mas são oxidados para produzir energia.
A desnutrição protéico-energética pode ocorrer secundariamente em crianças pelas seguintes razões:
- Perturbação dos processos digestivos (diminuição da absorção de nutrientes).
- A perda de proteínas pode ocorrer devido à regulação neuroendócrina.

Formulários
- Marasmo. Nesse caso, o crescimento da criança é retardado e observa-se gordura subcutânea.
- Kwashiorkor. Esta é precisamente uma deficiência proteica isolada. Além do retardo de crescimento, a criança pode apresentar inchaço e, porém, neste caso, permanece gordura subcutânea.
Gravidade
Se estamos falando de um problema como a desnutrição protéico-energética, o grau é o que também precisa ser falado. Existem apenas três deles:
- Fácil (primeiro, eu).
- Moderado (segundo, II).
- Pesado (terceiro, III).

Grau leve
Se estamos falando de um grau leve de deficiência protéica, o corpo da criança fica apenas enfraquecido. Nesse caso, sua resistência a diversos vírus e infecções diminui. Os principais sintomas que estarão presentes são:
- Fraqueza crescente.
- Letargia e baixa capacidade de trabalho da criança.
- Fadiga rápida não só física, mas também psicológica.
- Frieza, sensação de frio.
- Sede e fome. Pode haver aumento da micção.
- Tonturas são possíveis.
- Ocorrerá dormência nas extremidades inferiores.
O crescimento da criança também pode ser retardado nesta fase.
Grau moderado
Consideramos ainda um problema como a desnutrição protéico-energética. A doença do estágio 2 (primeiro) ocorre com mais frequência em residentes de países em desenvolvimento. Nesse caso, como mencionado acima, ocorre o crescimento dos filhos. Porém, o segundo grau também é caracterizado por alterações bioquímicas no corpo. Assim, ocorre um enfraquecimento celular significativo da imunidade. E isso leva ao aumento da sensibilidade a vários tipos de vírus e infecções.

Forma grave
Há também desnutrição protéico-energética profunda ou grave (ou seja, caquexia). No entanto, é mais comum em pessoas com câncer. Nesse caso, a criança pode perder peso muito rapidamente e ocorre diarreia. Os músculos do paciente também sofrem; os membros parecem gravetos cobertos de pele. O cabelo fica opaco, quebradiço e cai. Pode ocorrer retenção de água nos tecidos, muitas vezes levando ao inchaço. Mudanças irreversíveis também ocorrem nos órgãos internos do paciente. Porém, tudo isso é individual (o médico poderá informá-lo sobre isso após alguns estudos). Outros sintomas característicos de um problema como a desnutrição protéico-energética grave em crianças:
- Apatia, fadiga.
- Sensação constante de frio.
- Despigmentação da pele e dos cabelos.
- A pele fica seca e rachada. O rosto da criança ganha uma aparência antiga.
- A pressão arterial, o pulso e a temperatura diminuem.
Forma isolada
Bastante raro, mas ainda pode ocorrer uma forma isolada de deficiência protéica. Na maioria das vezes, é acompanhada por uma deficiência de componentes como vitaminas B1, B2, B6, ácido fólico e nicotínico, vitamina A. Se falamos de crianças, então a deficiência de vitamina A representa um perigo para as crianças. À medida que a doença progride, a deficiência intracelular ocorre perda de potássio, fósforo e magnésio.

Tratamento
Se falamos de um problema como a deficiência protéico-energética, é no tratamento que você também precisa focar sua atenção. Portanto, se a criança tiver uma das duas primeiras formas da doença, o problema ainda pode ser resolvido ajustando a dieta alimentar. Neste caso, é muito importante aumentar a ingestão diária de proteínas. Isso varia para crianças de diferentes idades:
- Se a criança tiver entre um e sete anos, a dose diária será de aproximadamente 3-4 gramas de proteína por 1 kg de peso.
- As necessidades proteicas dos alunos são ligeiramente inferiores: 2-3 gramas por 1 kg de peso.
A criança receberá complexos multivitamínicos. Afinal, só a comida neste caso não será suficiente. A regulação do equilíbrio hídrico e eletrolítico também pode ser realizada.
Se uma criança apresentar deficiência protéico-energética grave, o bebê será encaminhado ao hospital. É impossível lidar com esse problema sozinho em casa. O que será relevante neste caso:
- Dieta controlada.
- Correção do equilíbrio hidroeletrolítico por meio de terapia de infusão.
- Nutrição adicional também será prescrita com misturas ricas em nutrientes.
- Se a absorção estiver prejudicada, será prescrita à criança (infusão de nutrientes).
- Terapia vitamínica. Porém, neste caso será especial. Essas pessoas precisam do dobro de vitaminas que uma pessoa saudável. E isso até o momento da recuperação.
- Pacientes com anorexia podem receber medicamentos que aumentam o apetite. Se você precisar aumentar a massa muscular, os médicos podem prescrever esteróides anabolizantes.

Prevenção
Para evitar a desnutrição protéico-energética em crianças, é necessário monitorar cuidadosamente sua dieta. Os seguintes alimentos ajudarão a preencher sua alimentação com proteínas:
- Carne de frango.
- Peixe.
- Carne bovina.
- Ovos.
- Lacticínios.
Ao mesmo tempo, também é importante lembrar de outros microelementos úteis. Junto com as proteínas, a criança deve receber quantidades suficientes de carboidratos e gorduras dos alimentos.
NUTRIÇÃO PARA MALFICIÊNCIA ENERGÉTICA-PROTEICA (CID-10 E44)
Na Rússia, durante muitos anos, foi adotado o termo desnutrição, que é sinônimo de desnutrição protéico-energética.
A hipotrofia (estado nutricional prejudicado) é uma condição caracterizada por desnutrição crônica e falta de peso corporal em relação à altura e idade.
Dependendo do momento de ocorrência, é feita uma distinção entre desnutrição pré-natal (congênita, intrauterina) e pós-natal (desenvolvida após o nascimento). A desnutrição pré-natal baseia-se na violação do desenvolvimento intrauterino do feto devido às características constitucionais da mãe, insuficiência da circulação placentária, exposição a fatores infecciosos, hereditários, socioeconômicos, industriais e ambientais desfavoráveis.
No período pós-natal, a desnutrição pode desenvolver-se sob a influência de fatores endógenos ou exógenos (Tabela 24).
Tabela 24. Fatores predisponentes ao desenvolvimento de desnutrição no período pós-natal
|
Fatores endógenos |
Fatores exógenos |
|
Malformações congênitas (sistema cardiovascular, trato gastrointestinal, sistema nervoso central, sistema geniturinário, fígado) Lesões congênitas ou adquiridas do sistema nervoso central (isquemia cerebral, danos perinatais ao sistema nervoso, hemorragia intracraniana) Síndromes de má absorção (com deficiência de lactase, doença celíaca, fibrose cística, etc.) Imunodeficiências hereditárias Doenças endócrinas, etc. Distúrbios metabólicos hereditários |
Nutricional (desnutrição quantitativa e qualitativa, alimentação artificial precoce com fórmulas lácteas não adaptadas, introdução incorreta e inoportuna de alimentos complementares, irregularidades na alimentação e defeitos de cuidado) Curso crônico de doenças dependentes da nutrição (anemia, raquitismo, disbiose intestinal, etc.) Doenças infecciosas graves Patologia crônica grave |
Diagnóstico
Para identificar a desnutrição em crianças, são utilizados métodos clínicos e laboratoriais (Tabela 25).
Tabela 25. Métodos de avaliação do estado nutricional
Os métodos somatométricos são uma forma fundamental de avaliar o estado nutricional de uma criança. Um elemento necessário da antropometria é a presença de tabelas comparando os indicadores de peso-altura e idade e/ou um mapa da distribuição percentil dos indicadores de peso e altura. Em 2006, a Organização Mundial da Saúde propôs “Gráficos de Crescimento Padrão” para crianças de todas as faixas etárias para uso na prática pediátrica geral. Esses mapas contêm a distribuição das crianças por peso-idade, estatura-idade, indicadores peso-altura, bem como por índice de massa corporal.
Os pediatras nacionais classificam a desnutrição de acordo com o tempo de ocorrência e de acordo com a deficiência de peso corporal (Tabela 26).
Tabela 26. Classificação da desnutrição (de acordo com E.V. Neudakhin, 2001)
Um indicador mais objetivo do estado de desenvolvimento físico de uma criança de uma determinada idade é levar em consideração não só o peso corporal, mas também a altura. Para isso, é aconselhável utilizar tabelas de percentis. A deficiência combinada de peso corporal e altura se desenvolve com desnutrição prolongada ou com doença crônica grave da criança.
Em estudos epidemiológicos de prevalência de desnutrição infantil, é utilizado o indicador Z-score, que é o desvio dos valores de um indicador individual (peso corporal, altura, IMC) do valor médio de uma determinada população, dividido pelo desvio padrão do valor médio.
Em uma população padrão, o escore Z médio é zero com desvio padrão de 1,0. Valores positivos do escore Z indicam aumento do indicador antropométrico em relação ao padrão, e valores negativos indicam diminuição dos parâmetros em relação ao valor padrão. Por valores negativos pronunciados, pode-se julgar o atraso no desenvolvimento físico. Por exemplo, uma criança de 3 meses tem um peso corporal de 4 kg, enquanto o peso corporal médio de uma criança desta idade é de 6 kg.
Velocidade Z = (4 - 6)/1
De acordo com a fórmula, seu escore Z é -2, o que indica um atraso significativo no desenvolvimento físico.
A má nutrição e a perda de peso corporal manifestam-se não apenas pela deficiência proteico-calórica, mas também pela hipovitaminose, deficiência de muitos microelementos essenciais responsáveis pela implementação das funções imunológicas, pelo crescimento ideal e pelo desenvolvimento do cérebro. Portanto, a desnutrição a longo prazo é frequentemente acompanhada por um atraso no desenvolvimento psicomotor, atraso na fala e nas capacidades e funções cognitivas, e uma elevada incidência de doenças infecciosas devido à diminuição da imunidade, o que por sua vez agrava os distúrbios nutricionais.
As causas da desnutrição em diversas doenças em crianças podem ser divididas em 4 grupos:
nutrição insuficiente e desequilibrada, violação do regime alimentar;
desnutrição por dificuldade alimentar: doenças graves, disfagia, vômitos, paralisia cerebral e outros;
necessidades nutricionais aumentadas: bebês prematuros, defeitos cardíacos congênitos, patologia pulmonar crônica (displasia broncopulmonar, fibrose cística), período de reabilitação após infecções graves acompanhadas de estresse catabólico e outros.
violação da digestão e absorção de alimentos: síndrome de má absorção, todos os tipos de danos ao trato gastrointestinal (após cirurgia, doenças inflamatórias intestinais, síndrome de perda de proteínas intestinais, etc.)
Correção dietética da desnutrição
Regras básicas para organizar nutrição terapêutica para desnutrição:
é necessário levar em consideração a idade, gravidade, gravidade e natureza da doença de base;
esforçar-se por satisfazer as necessidades da criança em termos de nutrientes básicos, energia, macro e micronutrientes relacionadas com a idade, aumentando gradualmente a carga alimentar, tendo em conta a tolerância alimentar da criança;
evitar a substituição injustificada do leite humano ou de fórmulas lácteas adaptadas por produtos de alimentação complementar;
introduzir de forma consistente produtos de alimentação complementar, tendo em conta o estado nutricional da criança, aumentando gradualmente o seu volume;
utilizar produtos de alimentação complementar produzidos industrialmente; recomenda-se a introdução de cereais como primeira alimentação complementar.
Em caso de desnutrição de primeiro grau, é necessário estabelecer um regime geral, cuidar da criança e eliminar os defeitos alimentares. Na prescrição de alimentos, deve-se dar preferência ao leite materno, e no caso de alimentação mista e artificial - às fórmulas lácteas adaptadas enriquecidas com galacto e fruto-oligossacarídeos, que têm efeito benéfico nos processos digestivos e normalização da composição do microflora intestinal; nucleotídeos, que melhoram a absorção de nutrientes e estimulam o sistema imunológico da criança, além de produtos lácteos fermentados. Nesse caso, os cálculos e a correção nutricional são realizados com base no peso corporal adequado, que consiste no peso corporal ao nascer e na soma de seus aumentos normais ao longo da vida. Para aumentar o valor energético da dieta e aumentar a cota proteica, é possível prescrever refeições e alimentos complementares (mingaus, purês de vegetais e carne, requeijão) 2 semanas antes do que para crianças saudáveis.
No caso de desnutrição de segundo grau, a correção alimentar é convencionalmente dividida em três períodos: o período de adaptação (determinando a tolerância alimentar), o período de reparação (intermediário) e o período de nutrição melhorada.
Durante o período de adaptação, que dura de 2 a 5 dias, a nutrição é calculada com base no peso corporal real, de acordo com as necessidades fisiológicas da criança em nutrientes básicos e energia. O número de mamadas é aumentado em 1-2 por dia com uma redução correspondente no volume de cada mamada; é administrado líquido adicional (glicose a 5% ou soluções salinas para reidratação oral). Durante este período, juntamente com o leite humano ou fórmula infantil enriquecida com oligossacarídeos e nucleotídeos, é aconselhável utilizar misturas à base de hidrolisado protéico, de fácil digestão e absorção pelo organismo da criança, e misturas adaptadas de leite fermentado.
Com tolerância normal à nutrição prescrita, o volume das mamadas aumenta gradualmente (ao longo de 5 a 7 dias) até a norma fisiológica. É possível utilizar fórmulas com maior teor de proteínas, por exemplo, fórmulas lácteas especializadas para bebês prematuros. Com taxas suficientes de ganho de peso corporal e ausência de sintomas dispépticos, os cálculos nutricionais podem ser feitos com base no peso corporal adequado (peso corporal ao nascer + seu aumento normal ao longo da vida), primeiro nos componentes de carboidratos e proteínas, e só por último o componente gorduroso da dieta.
Durante o período de reparação é possível a introdução de alimentos complementares, começando pelos cereais produzidos industrialmente, seguidos da introdução de carne, requeijão e gema. Nesse período, devem ser prescritos preparados enzimáticos, complexos multivitamínicos e agentes que tenham efeito positivo nos processos metabólicos.
Ao longo do tratamento de crianças com desnutrição, é necessário o registro sistemático da nutrição real com cálculo da composição química da dieta diária com base nos principais nutrientes alimentares.
Na desnutrição grau III, todos os tipos de metabolismo são fortemente perturbados; o estado da criança, via de regra, é muito grave, por isso essas crianças necessitam de terapia intensiva e, muitas vezes, também do uso de nutrição não apenas enteral, mas também parenteral, que requer hospitalização tratamento. A hipotrofia grau III causada por fatores nutricionais é rara, pois os principais distúrbios na alimentação da criança são detectados precocemente e a necessária correção dietética da dieta dessas crianças é realizada mesmo nos graus I - II de desnutrição.
Táticas para manejo de pacientes com desnutrição grau III
Existem várias etapas táticas principais no tratamento da desnutrição grave no período inicial:
tratamento ou prevenção de hipoglicemia e hipotermia,
tratamento ou prevenção da desidratação e restauração do equilíbrio eletrolítico,
tratamento etiotrópico do processo infeccioso, se presente,
identificar e superar outros problemas associados à deficiência de vitaminas, microelementos, anemia, etc.
Para crianças que não necessitam de terapia urgente, a nutrição ideal é a base para um suporte nutricional adequado. Para evitar carga excessiva no trato gastrointestinal, rins e fígado, a alimentação deve ser iniciada em pequenas porções com pequenos intervalos entre as refeições (2,5-3 horas), desde que a criança se alimente de forma independente e mantenha o apetite. A capacidade energética da dieta deve fornecer no mínimo 80 kcal/kg e no máximo 100 kcal/kg/dia. Com uma ingestão calórica mais baixa, os processos de catabolismo continuam, enquanto com uma ingestão calórica mais elevada, podem desenvolver-se distúrbios metabólicos graves. À medida que a criança se adapta a esse conteúdo calórico, a quantidade de alimentos, a cota proteica e os intervalos entre as mamadas vão aumentando gradativamente. A quantidade de proteína na dieta nos primeiros dias de alimentação deve ser reduzida para 1,0-1,2 g/100 ml de mistura (Tabela 27).
|
Nutrientes |
Quantidade por kg de peso corporal/dia |
|
Eletrólitos: |
|
|
Microelementos: |
|
|
Vitaminas solúveis em água: Nicotiamida Ácido fólico Ácido pantotênico |
|
|
Vitaminas lipossolúveis |
|
Para crianças com comprometimento da função digestiva e de absorção do intestino (síndrome do intestino curto, diarreia persistente, doença inflamatória intestinal), a nutrição enteral deve começar com uma concentração muito baixa do produto; é melhor usar misturas contendo proteína hidrolisada, começando com uma Concentração de 3% do produto. A utilização de misturas contendo um componente proteico dividido em peptídeos (Alfare, Nutrilon Pepti TSC, Nutrilak Peptidi SCT, Pregestimil) dispensa o trabalho ativo das proteases e permite o fornecimento adequado de proteínas para os processos de reparação. A concentração da mistura administrada é aumentada lentamente, aumentando 1% ao dia (Tabela 28).
Tabela 28. Concentrações de mistura à base de hidrolisado protéico utilizada em crianças com desnutrição grave de terceiro grau
Além disso, a concentração da mistura é aumentada gradativamente para 13,5% e, se bem tolerada, para 15%. A falta de calorias, eletrólitos e nutrientes durante o período de consumo de um produto com baixa concentração de nutrientes é compensada pela nutrição parenteral. Para crianças gravemente enfermas, está indicada a infusão lenta e contínua de misturas nutricionais por sonda nasogástrica, o que promove o aproveitamento ideal dos nutrientes. Variando a taxa de infusão, o volume de digestão cavitária e absorção intestinal pode ser aumentado gradualmente. Este método de alimentação é eficaz e lógico para crianças com área de superfície de absorção reduzida, como atrofia das vilosidades intestinais, síndrome do intestino curto e outras condições.
A transição para a nutrição enteral fracionada pode levar de vários dias a várias semanas ou até meses, dependendo da gravidade da condição do paciente e da eficácia da infusão contínua. Durante o período de infusão, a sucção e a deglutição devem ser estimuladas simultaneamente. Ao mudar para refeições fracionadas, você pode primeiro deixar uma infusão constante à noite com refeições fracionadas simultâneas durante o dia em pequenas porções 5 a 6 vezes durante o dia, até que o conteúdo calórico das refeições fracionadas não exceda 75% da ingestão diária. A partir daí, passam totalmente para a nutrição fracionada, porém, a ingestão oral deve ser aumentada muito lentamente, pois a nutrição por infusão é acompanhada por uma diminuição relativa da atividade intestinal.
A melhora do apetite da criança e o aparecimento de ganho de peso indicam uma melhora no estado da criança. A partir deste momento inicia-se a fase de reabilitação, na qual se realiza uma transição gradual para uma dieta mais calórica e rica em proteínas, bem como a substituição das misturas hidrolisadas por misturas contendo proteínas integrais. O volume da alimentação fracionada deve ser aumentado lentamente em 10 ml a cada alimentação subsequente (por exemplo, 60 ml, depois 70 ml, depois 80 ml, etc.) até que o volume da nutrição atinja a norma da idade.
Nesse período, deve-se manter um gráfico de alimentação da criança, anotando os alimentos prescritos e efetivamente consumidos. Durante o período de reabilitação, a carga energética aumenta gradualmente de 80 - 100 kcal/kg/dia para 130 kcal/kg/dia com um consumo máximo de até 150 - 200 kcal/kg/dia. Caso a criança não consiga digerir a ingestão nutricional de 130 kcal/kg/dia, reverter para volumes menores, maior frequência e até infusões contínuas de soluções nutricionais se necessário. A duração do período de reabilitação depende da idade, da gravidade da doença de base e da velocidade de adaptação da criança à alimentação. Ao mesmo tempo, aumente a cota de proteína na dieta de 1 para 2,5 - 3,0 g/100 ml. Os critérios para adequação do suporte nutricional são: melhora do apetite, bem-estar geral, atividade física e ganho de peso diário de pelo menos 5 g/kg de peso corporal por dia.
Os materiais para este capítulo também foram fornecidos por: Bushueva T.V. (Moscou), Rybakova E.P. (Moscou), Stepanova T.N. (Moscou)
RCHR (Centro Republicano para o Desenvolvimento da Saúde do Ministério da Saúde da República do Cazaquistão)
Versão: Protocolos clínicos do Ministério da Saúde da República do Cazaquistão - 2015
Marasmo nutricional (E41), Desnutrição protéico-energética, não especificada (E46), Desnutrição protéico-energética moderada e leve (E44), Atraso no desenvolvimento devido à desnutrição protéico-energética (E45), Kwashiorkor (E40), Kwashiorkor marásmico (E42), Desnutrição protéico-energética grave, não especificada (E43)
Gastroenterologia Pediátrica, Pediatria
informações gerais
Pequena descrição
Recomendado
Conselho de profissional
RSE no RVC "Centro Republicano"
desenvolvimento da saúde"
Ministério da Saúde
e desenvolvimento social
República do Cazaquistão
datado de 6 de novembro de 2015
Protocolo nº 15
Nome do protocolo: Deficiência protéico-energética em crianças
Deficiência protéico-energética- desnutrição da criança, caracterizada por interrupção ou desaceleração do ganho de peso corporal, diminuição progressiva do tecido subcutâneo, distúrbios nas proporções corporais, funções nutricionais, metabolismo, enfraquecimento das defesas específicas e inespecíficas e astenização do corpo, um tendência a desenvolver outras doenças, atrasos no desenvolvimento físico e neurológico, desenvolvimento mental.
Código do protocolo:
Código(s) CID-10:
· E40-E 46. Desnutrição (hipotrofia: pré-natal, pós-natal).
· E40. Kwashiorkor.
·E41. Insanidade nutricional.
·E42. Kwashiorkor senil.
· E43. Desnutrição protéico-energética grave, não especificada.
· E44. Desnutrição protéico-energética, não especificada, moderada e fraca.
·E45. Atraso no desenvolvimento causado por deficiência protéico-energética.
· E46. Desnutrição protéico-energética, não especificada.
Abreviações usadas no protocolo:
|
PEM - desnutrição protéico-energética ACTH - hormônio adrencorticotrófico AMK - aminoácido AST- aspartato aminotransferase Alt - alanina aminotransferase AT para TTG - anticorpos para transglutaminase tecidual DII - doenças inflamatórias intestinais PRV - má-formação congênita UPS - Defeito cardíaco congênito DRGE - doença do refluxo gastroesofágico Trato gastrointestinal - trato gastrointestinal IMC - índice de massa corporal TC - Tomografia computadorizada KFK- creatina fosfoquinase Terapia por exercício - fisioterapia FC - fibrose cística NS - sistema nervoso PP- nutrição parenteral SCT- triglicerídeos de cadeia média 17-OX - 17-cetosteroides TSH- hormônio estimulador da tireoide Ultrassom - ultrassonografia FGDS- fibroesofagogastroduodenoscopia fosfato alcalino - fosfatase alcalina SNC - sistema nervoso central ECG - eletrocardiograma EcoCG Ecocardiografia |
Data de desenvolvimento do protocolo: 2015
Usuários do protocolo: pediatras, clínicos gerais, neurologistas pediátricos, gastroenterologistas, endocrinologistas, cirurgiões, oncologistas, hematologistas, pneumologistas, reanimadores.
Avaliação do grau de evidência das recomendações fornecidas.
Escala de nível de evidência:
| A | Uma metanálise de alta qualidade, revisão sistemática de ECRs ou ECRs grandes com probabilidade muito baixa (++) de viés, cujos resultados possam ser generalizados para uma população apropriada. |
| EM | Revisão sistemática de alta qualidade (++) de estudos de coorte ou caso-controle ou estudos de coorte ou caso-controle de alta qualidade (++) com risco muito baixo de viés ou ECRs com risco baixo (+) de viés, os resultados de que pode ser generalizado para uma população apropriada. |
| COM |
Estudo de coorte ou caso-controle ou ensaio controlado sem randomização com baixo risco de viés (+). Resultados que podem ser generalizados para a população relevante ou ECRs com risco de viés muito baixo ou baixo (++ ou +) cujos resultados não podem ser generalizados diretamente para a população relevante. |
| D | Série de casos ou estudo não controlado ou opinião de especialistas. |
| PPG | Melhores práticas farmacêuticas. |
Classificação
Classificação clínica:
Por hora de ocorrência:
· pré-natal;
· pós-natal.
Por etiologia:
· nutricional;
· infeccioso;
· associado a defeitos no regime e na dieta;
· associado a fatores prejudiciais ao pré-natal;
· causada por patologia hereditária e anomalias congênitas do desenvolvimento.
Por gravidade:
· PEM grau I - deficiência de peso corporal 11-20%;
· Grau PEM II - deficiência de peso corporal 21-30%;
· Grau PEM III - deficiência de peso corporal › 30%.
Por períodos:
· inicial;
· progressão;
· estabilização;
· convalescença.
Por formulário:
Aguda - manifesta-se por perda predominante de peso corporal e sua deficiência em relação ao peso corporal necessário para estatura;
· crónica - manifestada não só pela falta de peso corporal, mas também por um atraso significativo no crescimento.
Algumas variantes especiais da variedade BEN:
· kwashiorkor, marasmo nutricional, kwashiorkor marasmático;
· desnutrição em crianças mais velhas;
· falta de microelementos (cobre, zinco, selênio).
Quadro clínico
Sintomas, claro
Critérios diagnósticos para diagnóstico
:
Reclamações e anamnese:
Reclamações: dependendo da patologia que levou aos sinais de desnutrição: baixo ganho de peso e altura, falta de apetite, recusa em comer, vômitos, náuseas, engasgos durante a alimentação, distensão abdominal, fezes moles, prisão de ventre, grande volume de fezes, dor abdominal, inchaço, cólicas , tosse, falta de ar, febre prolongada, ansiedade, pele seca, queda de cabelo, deformação das unhas, fraqueza.
Anamnese: Determine a doença na criança que levou aos sinais de PEM.
Tabela 1 - Principais causas da desnutrição infantil
| causas | mecanismos | nosologias e condições |
| Ingestão alimentar insuficiente | distúrbios de deglutição (disfagia), anorexia, distúrbios de consciência, hemorragia intracraniana, insuficiência cardíaca ou respiratória crônica, subalimentação, desnutrição em adolescentes | não fechamento do palato mole e duro, tumores da cavidade oral e faringe, distúrbios anatômicos do trato gastrointestinal (refluxo gastroesofágico, piloroespasmo, estenose pilórica), cardiopatia congênita, malformação congênita dos pulmões, malformação congênita do SN, síndrome adrenogenital, anorexia psicogênica |
| Distúrbios digestivos e de absorção de nutrientes (má digestão e má absorção) | distúrbios da digestão e absorção de proteínas, gorduras, carboidratos, micro-macronutrientes | fibrose cística, doença celíaca, acrodermatite enteropática, enteropatias alérgicas, transporte prejudicado de glicose - galactose, estados de imunodeficiência, síndrome do intestino curto, linfangiectasia, diarreia por cloreto, malformação congênita do intestino delgado e grosso |
| Perda de nutrientes do corpo | perda de proteínas, vitaminas, macro e microelementos - através do trato gastrointestinal ou rins | fístulas intestinais, diarreia profusa, vômitos incontroláveis, síndrome de Bartter, DII |
| Distúrbios metabólicos | estados catabólicos, disfunções orgânicas | lesões graves, sepse, processo oncológico, leucemia, insuficiência hepática, renal |
Critérios clínicos:
· avaliação do estado físico (cumprimento dos padrões de idade em termos de peso, comprimento corporal, etc.) através de tabelas de percentis;
· avaliação do estado somático e emocional (vivacidade, reação ao meio ambiente, morbidade, etc.);
· avaliação da pele (palidez, ressecamento, presença de erupções cutâneas, etc.);
· avaliação do estado das mucosas (presença de aftas, candidíase, etc.);
· avaliação do turgor tecidual;
O peso corporal adequado (ideal) em crianças é determinado por meio de tabelas de distribuições percentuais ou percentuais do peso corporal, dependendo da altura, idade e sexo da criança. Ao estudar parâmetros antropométricos em crianças, avalia-se a circunferência da cabeça, tórax, abdômen, ombro, quadril, bem como a espessura da pele e dobras de gordura em pontos padrão. Em crianças pequenas, é dada grande importância ao perímetro cefálico, ao número de dentes e ao tamanho das fontanelas.
Tabela 2 - Classificação da desnutrição protéico-energética em crianças pequenas (segundo Waterlow J.C., 1992)
Tabela 3 - Avaliação do estado nutricional em crianças maiores de 12 anos por índice de massa corporal (Gurova M.M., Khmelevskaya I.G., 2003)
| Tipo de transtorno alimentar | grau | Índice de massa corporal |
| Obesidade | EU | 27,5-29,9 |
| II | 30-40 | |
| III | >40 | |
| Maior nutrição | 23,0-27,4 | |
| Norma | 19,5-22,9 | |
| Nutrição reduzida | 18,5-19,4 | |
| BEN | EU | 17-18,4 |
| II | 15-16,9 | |
| III | <15 |
Avaliação da camada de gordura subcutânea (redução ou ausência):
· com PEN estágio I - redução do abdômen;
· com grau PEN II - diminuição do abdômen, membros;
· com PEN grau III - ausência na face, abdômen, tronco e membros.
Exame físico e laboratorial: atraso no desenvolvimento físico e neuropsíquico.
BEN 1º grau- nem sempre é diagnosticado, pois o estado geral da criança sofre pouco. Sintomas: inquietação motora moderada, diminuição dos movimentos intestinais, leve palidez da pele, adelgaçamento da gordura subcutânea no tronco e/ou abdômen. Na região do umbigo, a camada de gordura subcutânea atinge 0,8 - 1,0 cm e o peso corporal é reduzido em 10-20% do seu valor normal. IMC - 17 - 18,4. O índice de condição corporal de Chulitskaya atinge 10-15 (normalmente 20-25). O desenvolvimento psicomotor corresponde à idade, a reatividade imunológica e a tolerância alimentar não são alteradas. No espectro de proteínas do sangue há hipoalbuminemia. Sintomas de raquitismo, anemia por deficiência.
BENII grau- caracterizado por alterações pronunciadas em todos os órgãos e sistemas. Diminuição do apetite, vômitos periódicos, distúrbios do sono. Há um atraso no desenvolvimento psicomotor: a criança não segura bem a cabeça, não senta, não fica de pé e não anda. Os distúrbios da termorregulação se manifestam por flutuações significativas na temperatura corporal durante o dia. Um afinamento acentuado da gordura subcutânea no abdômen, tronco e membros. A dobra cutânea na região do umbigo é de 0,4-0,5 cm, o índice Chulitskaya diminui para 10,0. A diferença no peso é de 20 a 30%, no comprimento do corpo é de 2 a 4 cm e o IMC é de 15 a 16,9. Tipo incorreto de curva de crescimento de massa. A pele é pálida, acinzentada pálida, notando-se ressecamento e descamação da pele (sinais de poli-hipovitaminose). A elasticidade, o turgor dos tecidos e o tônus muscular diminuem. O cabelo fica opaco e quebradiço. A tolerância alimentar diminui. A natureza dos movimentos intestinais muda - fezes instáveis, alternância de constipação e diarréia. Amido, gordura neutra, muco, fibras musculares e distúrbios na flora intestinal podem ser detectados nas fezes. A urina cheira a amônia. Patologia somática concomitante (pneumonia, otite média, pielonefrite), condições de deficiência.
BENIII grau- anorexia, letargia geral, diminuição do interesse pelo meio ambiente, falta de movimentos ativos. O rosto está sofrendo, senil, as bochechas estão encovadas com a atrofia dos caroços de Bisha, no período terminal - indiferença. A termorregulação fica gravemente prejudicada, a criança esfria rapidamente. Dobra de pele na altura do umbigo até 0,2 cm (quase desaparece). O índice de condição corporal de Chulitskaya é negativo. A defasagem no peso corporal é superior a 30%, a defasagem no comprimento do corpo é superior a 4 cm e atraso no desenvolvimento psicomotor. IMC -<15 Дыхание поверхностное, иногда могут отмечаться апноэ. Тоны сердца ослабленные, глухие, может наблюдаться тенденция к брадикардии, артериальной гипотонии. Живот увеличен в объёме вследствие метеоризма, передняя брюшная стенка истончена, контурируются петли кишок, запоры чередуются с мыльно-известковыми испражнениями. Резко нарушена толерантность к пище, нарушены все виды обмена. У большинства больных отмечается рахит, анемия, явления дисбиоза. Терминальный период характеризуется триадой: гипотермией (температура тела 32-33° С), брадикардией (60-49 уд/мин), гипогликемией.
As manifestações clínicas do PEM são agrupadas em síndromes:
· síndrome de distúrbios tróficos: adelgaçamento do tecido adiposo subcutâneo, diminuição do turgor tecidual, curva de crescimento plana e deficiência de peso corporal em relação ao comprimento corporal, sinais de polihipovitaminose e hipomicroelementose;
· síndrome de distúrbios digestivos: anorexia, distúrbios dispépticos, diminuição da tolerância alimentar, sinais de má digestão no coprograma;
· síndrome de disfunção do sistema nervoso central: diminuição do tônus emocional, predomínio de emoções negativas, ansiedade periódica (com PEN estágio III - apatia), atraso no desenvolvimento psicomotor;
· síndrome de distúrbios hematopoiéticos e diminuição da reatividade imunobiológica: anemia deficiente, estados de imunodeficiência secundária (o componente celular da imunidade é especialmente afetado). É observado um curso apagado e atípico de processos patológicos.
Diagnóstico
Testes de diagnóstico:
Exames diagnósticos básicos (obrigatórios) realizados em regime ambulatorial:
· análise geral de sangue;
· análise geral de urina;
· coprograma;
· exame bioquímico de sangue: proteína total, bilirrubina total e suas frações, ALT, AST, glicose;
Pesando e medindo o comprimento do corpo da criança
A lista mínima de exames que devem ser realizados no encaminhamento para internação planejada: de acordo com o regulamento interno do hospital, atendendo à ordem vigente do órgão autorizado na área da saúde.
Exames diagnósticos básicos (obrigatórios) realizados em nível de internação (durante a internação planejada):
· exame de sangue geral (uma vez a cada 10 dias);
· análise geral de urina (uma vez a cada 10 dias);
· exame bioquímico de sangue: proteínas totais, frações proteicas, bilirrubina total e suas frações, ALT, AST, glicose, fosfatase alcalina, níveis de eletrólitos (potássio, sódio, magnésio, fósforo, cálcio, cloro), uréia, transferrina, creatinina, colesterol;
· coprograma;
· ECG;
· EcoCG;
· Ultrassonografia dos órgãos abdominais, rins, glândulas supra-renais;
· monitoramento e análise da nutrição real – diariamente;
Testes de diagnóstico adicionais realizadosno nível estacionário:
· determinação de cloretos no suor;
· determinação de anticorpos anti-transglutaminase tecidual (AT para TTG) através do teste “Biocard celíaco”;
· semeadura de fluidos biológicos com seleção de colônias;
· análise da sensibilidade microbiana aos antibióticos;
· coagulograma;
· imunograma (número total de linfócitos, linfócitos T CD4+, granulócitos, atividade do complemento, imunoglobulinas A, M, G);
· hormônios da glândula tireóide (TSH, T3, T4), glândulas supra-renais (cortisol, ACTH, 17 OCS), CPK;
· FGDS com biópsia;
· exame histológico da membrana mucosa do jejuno;
· TC (cabeça, tórax, órgãos abdominais, pélvicos);
excreção diária de sal;
· pesquisa genética (conforme prescrição do geneticista);
· Exame radiográfico do tórax e órgãos abdominais;
· consultas com especialistas: pneumologista, gastroenterologista, imunologista,
oncologista, neurologista, hematologista, endocrinologista, psicólogo médico, psiquiatra, cirurgião, cirurgião cardíaco, infectologista, geneticista, nutricionista, reanimador.
Estudos instrumentais:
· ECG – para diagnóstico de triagem;
· EchoCG - para fins diagnósticos para identificação de alterações morfológicas e funcionais do coração;
· exame ultrassonográfico da cavidade abdominal, rins - para diagnóstico de triagem.
· A fibroesofagogastroduodenoscopia com biópsia do intestino delgado é realizada para fins diagnósticos em crianças com síndrome de má absorção.
· A fibroesofagogastroduodenoscopia é realizada para fins diagnósticos em crianças com regurgitação ou vômito.
· Exame radiográfico do esôfago, estômago, vias biliares, intestinos, pulmões - para excluir malformação congênita.
· Tomografia computadorizada da cabeça, tórax, órgãos abdominais e pélvicos - para excluir um processo patológico.
Pesquisa laboratorial:
· determinação de cloretos no suor - se houver suspeita de fibrose cística;
· determinação de anticorpos anti-transglutaminase tecidual (AT para TTG) através do teste “Biocard celíaco” - em caso de má absorção, para excluir doença celíaca;
· semeadura de fluidos biológicos com seleção de colônias - durante um processo infeccioso de longa duração;
· análise da sensibilidade dos micróbios aos antibióticos - para a seleção da terapia antimicrobiana racional;
· coagulograma - para diagnóstico do sistema de hemostasia;
· imunograma (número total de linfócitos, linfócitos T CD4 +, granulócitos, atividade do complemento, imunoglobulinas A, M, G) - para excluir um estado de imunodeficiência;
· hormônios da glândula tireóide (TSH, T3, T4), glândulas supra-renais (cortisol, ACTH, 17 OKS), CPK - para excluir patologia da glândula tireóide e glândulas supra-renais;
excreção diária de sal - para o diagnóstico de distúrbios metabólicos.
Diagnóstico diferencial
Diagnóstico diferencial:
Ao examinar e examinar uma criança com PEM, a causa que levou ao PEM é determinada e uma patologia concorrente é excluída.
Nesse sentido, é necessário diferenciar as seguintes doenças:
· doenças infecciosas;
· doenças crônicas do aparelho broncopulmonar;
· enzimopatias hereditárias e congênitas;
· doenças endócrinas;
doenças orgânicas do sistema nervoso central;
· doenças cirúrgicas;
· doenças genéticas;
· doenças que ocorrem com síndrome de má absorção;
· patologia oncológica.
Tratamento no exterior
Receba tratamento na Coréia, Israel, Alemanha, EUA
Obtenha conselhos sobre turismo médico
Tratamento
Metas de tratamento:
· eliminação dos fatores que levaram ao PEM;
· estabilização da condição da criança;
· dietoterapia otimizada;
· terapia de reposição (enzimas, vitaminas, microelementos);
· restauração do estado imunológico reduzido;
· tratamento de doenças e complicações concomitantes;
· organização de regime ideal, cuidados, massagem, terapia por exercícios;
Táticas de tratamento:
· crianças com PEM estágio 1, na ausência de doenças concomitantes graves e complicações, são indicadas para tratamento ambulatorial;
· crianças com graus PEM II - III, dependendo da gravidade do quadro, são indicadas para exame e tratamento hospitalar;
· no tratamento de crianças com PEN estágio III, com sinais de falência de múltiplos órgãos, para correção da terapia infusional e nutrição parenteral em curso, internação em unidade de terapia intensiva;
· o tratamento da PEM em crianças mais velhas inclui os mesmos princípios gerais do tratamento da PEM em crianças pequenas. Para crianças em idade escolar, a dietoterapia utilizada para PEM em adultos é aceitável, mas levando em consideração as necessidades de nutrientes, ingredientes, calorias relacionadas à idade e as características individuais da criança doente.
Tratamento não medicamentoso:
· horário ideal de sono, de acordo com a idade, permanência em ambiente bem ventilado e iluminado, a limpeza úmida é realizada duas vezes ao dia. A temperatura do ar deve ser mantida na sala (enfermaria) na faixa de 25-26° C.
· dietoterapia: misturas à base de hidrólise profunda da proteína do leite, com MCT, sem lactose, alto teor calórico (Nutrilon Petit Gastro, Alfare, Humana HN MCT; para crianças maiores de um ano: Nutricomp Energy, Nutricomp Energy Fiber, Nutrien Elemental, Fresubin Energy, Diben, Reconvan, Nutrien Immun, Supportan, Pedia Shur Misturas para prematuros à base de hidrólise parcial de proteínas, com MCT, alto teor calórico: Humana O-NA, Pre Nutrilon, Pre Nan, Similac Cuidados especiais;
Tratamento medicamentoso:
Medicamentos essenciais (Tabela 8):
Preparações enzimáticas - medicamentos que ajudam a melhorar o processo de digestão e incluem enzimas digestivas (enzimas). As mais ideais são as formas microesféricas e microencapsuladas de pancreatina. As preparações enzimáticas são prescritas a longo prazo na proporção de 1.000 unidades/kg por dia nas refeições principais.
Vitaminas solúveis em gordura, solúveis em água- para correção de deficiências (ácido ascórbico, vitaminas B, vitamina A, E, D, K), para administração parenteral - Addamel, Vitalipid.
Antibióticos - Vários grupos de antibióticos são usados para prevenir e tratar infecções .
Probióticos - microrganismos vivos que constituem a flora normal do trato intestinal humano. Em crianças com PEM, são observados processos disbióticos. São prescritas preparações probióticas - contendo bactérias lacto e bifido (Bifiform, Lacidofil, Normobakt).
Suplementos de ferro - usado para PEM para corrigir a deficiência de ferro (Totema, Aktiferrin, Ranferon).
Medicamentos que repõem a deficiência de hormônio tireoidiano recomendado para condições hipotireoidianas de diversas etiologias.
Glicocorticóides têm um efeito antiinflamatório, antialérgico, antichoque e antitóxico pronunciado.
Drogas imunológicas, usado para terapia de reposição e imunomoduladora. Reduzem o risco de desenvolver infecções na imunodeficiência primária e secundária, enquanto os anticorpos possuem todas as propriedades características de uma pessoa saudável e são utilizados como terapia de reposição em crianças - Octagam 10%.
Medicamentos de reposição plasmática destinado à correção de distúrbios graves do metabolismo protéico (hipoproteinemia), restauração da pressão colóide-oncótica, comprometimento hemodinâmico - solução de albumina 5%, 10%, 20%).
Soluções de aminoácidos - soluções nutricionais especiais para nutrição parenteral de crianças, para pacientes com insuficiência renal aguda e crônica, pacientes com diversas doenças hepáticas e para o tratamento de encefalopatia hepática. Soluções de infusão constituídas por eletrólitos e aminoácidos, que são análogos metabólicos ou substâncias fisiológicas para a formação de proteínas. Equilibrado no conteúdo de aminoácidos essenciais e não essenciais - Infezol 40, Infezol 100, Aminoplasmal E 5%, 10%, Aminoven infantil 10%.
Emulsões gordurosas- o uso de emulsões gordurosas fornece ao corpo ácidos graxos poliinsaturados e ajuda a proteger a parede das veias da irritação por soluções hiperosmolares. Uma fonte de energia que inclui um componente lipídico de fácil utilização (triglicerídeos de cadeia média) - fornecendo ao corpo ácidos graxos essenciais como parte da nutrição parenteral - Lipofundin MCT\LCT, Intralipid 20%, SMOFlipid 20%.
Solução de glicose- a glicose está envolvida em vários processos metabólicos do corpo, 5%, 10%, 20%.
Drogas combinadas - incluem recipientes combinados para administração parenteral: “dois em um” de dois componentes (solução AMK e solução de glicose), “três em um” de três componentes (solução AMK, solução de glicose e emulsão de gordura), também (solução AMK , solução de glicose, emulsão gordurosa com inclusão de ácidos graxos ômega 3) - Oliclinomel, SmofKabiven central, SMOF Kabiven periférico.
Tratamento medicamentoso realizado em regime ambulatorial:
Para PEM de 1 a 2 graus, a dietoterapia tradicional é realizada com mudança gradual na dieta, destacando:
· fase de adaptação, alimentação cuidadosa e tolerante;
· estágio de nutrição reparadora (intermediária);
· estágio de nutrição ideal ou aprimorada.
Durante o período de determinação da tolerância alimentar, a criança se adapta ao volume necessário e corrige o metabolismo água-mineral e proteico. Durante o período de reparação, o metabolismo de proteínas, gorduras e carboidratos é corrigido e, durante o período de aumento da nutrição, a carga energética aumenta.
Para o PEM, nos períodos iniciais do tratamento, reduzir o volume e aumentar a frequência da alimentação. A quantidade diária de alimento necessária para uma criança desnutrida é de 200 ml/kg, ou 1/5 do seu peso corporal real. O volume de líquido é limitado a 130 ml/kg por dia, e em caso de edema grave - a 100 ml/kg por dia.
Com o PEN estágio I, o período de adaptação geralmente dura de 2 a 3 dias. No primeiro dia, são prescritos 2/3 da quantidade diária necessária de alimentos. Durante o período de determinação da tolerância alimentar, seu volume aumenta gradativamente. Ao atingir a quantidade diária necessária de alimentos, é prescrita nutrição aprimorada. Neste caso, a quantidade de proteínas, gorduras e carboidratos é calculada para o peso corporal adequado (digamos que a quantidade de gordura é calculada para o peso corporal médio entre o real e o esperado).
Tabela 4 - Tratamento dietético do PEM estágio 1
| número de mamadas | conteúdo calórico, kcal/kg/dia | proteínas, g\kg\dia | gorduras, g\kg\dia | carboidratos\g\kg\dia |
|
de acordo com a idade n = 5-6 (10) |
cálculos de acordo com idade e peso adequado Peso corporal adequado = peso corporal ao nascer + a soma de seus aumentos normais ao longo da vida |
|||
| 0-3 meses 115 | 2,2 | 6,5 | 13 | |
| 4-6 meses 115 | 2,6 | 6,0 | 13 | |
| 7-12 meses 110 | 2,9 | 5,5 | 13 | |
No caso do PEN estágio II, 1/2-2/3 da quantidade diária necessária de alimentos é prescrita no primeiro dia. A quantidade de alimento que falta é reposta com a ingestão de soluções de reidratação. O período de adaptação termina quando a quantidade diária necessária de alimento é atingida.
Tabela 5 - Cálculo da nutrição para grau PEM II durante o período de adaptação
Com tolerância normal, inicia-se um período de reparação, quando o volume da nutrição aumenta gradativamente (ao longo de 5 a 7 dias), enquanto o cálculo dos nutrientes é feito com base no peso corporal adequado. Primeiro, os componentes de carboidratos e proteínas da dieta aumentam, depois o componente de gordura. Isso se torna possível com a introdução de alimentos complementares: cereais sem laticínios, carnes e purês de vegetais.
Tabela 6 - Cálculo da nutrição para PEN estágio II durante o período de reparo
Durante o período de nutrição aprimorada, o teor de proteínas e carboidratos aumenta gradativamente, sua quantidade passa a ser calculada com base no peso adequado, a quantidade de gordura - no peso médio entre o real e o esperado. Ao mesmo tempo, a carga de energia e proteína no peso corporal real excede a carga em crianças saudáveis. Isto se deve a um aumento significativo no consumo de energia em crianças durante o período de convalescença com PEM.
Tabela 7 - Cálculo da nutrição para PEN estágio II durante o período de nutrição melhorada
No futuro, a alimentação da criança se aproxima dos parâmetros normais, ampliando a gama de produtos, aumentando o volume diário de alimentos consumidos e reduzindo o número de mamadas. Período de nutrição melhorada, durante o qual a criança recebe nutrição hipercalórica (130-145 kcal/kg/dia) em combinação com medicamentos que melhoram a digestão e absorção dos alimentos. O volume de alimentação deve ser aumentado gradualmente sob estrito monitoramento da condição da criança (pulso e frequência respiratória). Se bem tolerado, na fase de nutrição melhorada, é fornecida nutrição hipercalórica (150 kcal/kg por dia) com maior teor de nutrientes, mas a quantidade de proteínas não excede 5 g/kg por dia, gorduras - 6,5 g/kg por dia, carboidratos - 14-16 g/kg por dia. A duração média do estágio de nutrição aprimorada é de 1,5 a 2 meses.
Para corrigir a deficiência de micronutrientes característica de qualquer forma de PEM, são utilizadas formas farmacêuticas de vitaminas e microelementos. Isto requer uma abordagem extremamente equilibrada. Apesar da incidência bastante elevada de anemia no PEM, os suplementos de ferro não são utilizados nas fases iniciais da amamentação. A correção da sideropenia é realizada somente após estabilização do quadro, na ausência de sinais de processo infeccioso, após restauração das funções básicas do trato gastrointestinal, apetite e ganho de peso persistente, ou seja, não antes de 2 semanas a partir do início da terapia. Caso contrário, esta terapia pode aumentar significativamente a gravidade da doença e piorar o prognóstico se a infecção se desenvolver.
Para corrigir a deficiência de micronutrientes é necessário fornecer ferro na dose de 3 mg/kg por dia, zinco 2 mg/kg por dia, cobre - 0,3 mg/kg por dia, ácido fólico (no primeiro dia - 5 mg, e depois - 1 mg/kg por dia) seguido de prescrição de preparações multivitamínicas, tendo em conta a tolerância individual.
Tabela 8 – Medicamentos essenciais:
| Nome | Gama terapêutica | Um curso de tratamento |
| Mistura “Nutrilon Pepti Gastro”, “Alfare”, “Nutrilak Peptidi TSC”, misturas para prematuros, misturas para crianças maiores de 1 ano “Nutrien Elemental”, “Nutrien Immun” (UD - A) | cálculo dependendo do período de adaptação |
correção individual, 2-3 meses Dependendo das manifestações clínicas, para FC - para toda a vida (ver protocolo de tratamento de FC) Longo prazo, 3-6 meses Duração do curso 2-3 meses Duração 1 mês Duração 2 meses Duração 2 meses Duração 1 mês |
| Pancreatina (UD - B) | 1.000 U\kg por dia de lipase, com CF 6.000-10.000 UI\kg\dia para lipase | |
| Colecalciferol (UD - B) | 500-3000 U/dia, 1-4 gotas 1 vez por dia | |
| Sulfato ferroso (UD - A) | 4 mg\kg 3 vezes ao dia, por via oral | |
| Retinol | necessidade diária de vitamina A para crianças: menores de 1 ano - 1.650 UI (0,5 mg), de 1 ano a 6 anos - 3.300 UI (1 mg), a partir de 7 anos - 5.000 UI (1,5 mg). | |
| Tocoferol (UD - A) | para crianças com mais de 10 anos, a dose diária de vitamina é de 8 a 10 mg; para crianças menores de 3 anos, a dose diária é de 3 a 6 mg; para crianças menores de 10 anos, não mais que 7 mg . | |
| Ácido fólico (UD - A) | dose de manutenção para recém-nascidos - 0,1 mg/dia; para crianças menores de 4 anos - 0,3 mg/dia; para crianças maiores de 4 anos e adultos - 0,4 mg/dia. Para hipo e deficiência de vitaminas (dependendo da gravidade da deficiência de vitaminas): idade 12 anos - até 5 mg/dia; crianças - em doses menores dependendo da idade | |
|
Sulfato de zinco (UD - B) |
2-5 mg/dia | |
| Preparações contendo microrganismos antidiarreicos (Lactobacillus, Bifidobacterium, esporos de Bacillus clausii) (UD - C) | na dosagem de idade |
Tratamento medicamentoso fornecido em nível de internação:
dependendo da causa que levou ao PEM. No caso dos graus PEN II - III, é fornecido suporte nutricional abrangente por meio de nutrição enteral e parenteral.
Um tipo justificado de nutrição enteral nas formas graves de PEM é a alimentação por sonda enteral de longo prazo, que consiste em um fornecimento lento e contínuo de nutrientes ao trato gastrointestinal (estômago, duodeno, jejuno - gotejamento, de forma ideal - usando uma bomba de infusão).
Tabela 9 - Cálculo da nutrição para PEN estágio III durante o período de adaptação
Tabela 10 - Cálculo da nutrição para PEN estágio III durante o período de reparo
Alimentos complementares hipercalóricos são introduzidos gradativamente na alimentação da criança, sendo possível a introdução de fórmulas adaptadas de leite fermentado.
Com boa tolerância à dieta prescrita na fase de nutrição melhorada, o conteúdo calórico aumenta para 130-145 kcal/kg/dia por peso corporal adequado, com aumento do teor de nutrientes, mas não mais: proteínas - 5 g/kg/ dia, gorduras - 6,5 g /kg/dia, carboidratos - 14-16 g/kg/dia. A duração média da fase de nutrição melhorada é de 1,5 a 2 meses (ver Tabela 7).
Tabela 11 - Indicadores de adequação da dietoterapia
Tabela 12 - Medicamentos essenciais em nível hospitalar
Para corrigir as principais síndromes, recomenda-se:
| POUSADA | Gama terapêutica | Um curso de tratamento | ||
|
Correção de distúrbios do metabolismo das proteínas: 1) Presença de edema hipoproteinêmico, restauração da pressão oncótica |
||||
| Solução de albumina 10% | 3-10ml/kg/dia IV, gotejamento | até que o efeito seja alcançado sob o controle de um proteinograma e parâmetros hemodinâmicos | ||
| 2) Nutrição parenteral | ||||
| Soluções de aminoácidos | 2-5 anos - 15 ml/kg/dia, 6-14 anos -10 ml/kg/dia IV, gotejamento | até que o efeito seja alcançado sob o controle do equilíbrio hídrico e dos níveis de eletrólitos no soro sanguíneo | ||
| Emulsões gordurosas |
0,5 - 2,0 g\kg/dia, por via intravenosa, gotejamento |
até que o efeito seja alcançado sob o controle das concentrações plasmáticas de triglicerídeos | ||
| Correção de processos metabólicos realizado no contexto da restauração dos níveis de proteína no sangue: | ||||
| Orotato de potássio | 10-20 mg/kg/dia por via oral | 3-4 semanas | ||
| Levocarnitina |
>12 anos 2-3 g/dia 6-12 anos - 75 mg/kg/dia, 2-6 anos - 100 mg/kg/dia, até 2 anos - 150 mg/kg/dia por via oral |
3-4 semanas | ||
| Correção de distúrbios hídricos e eletrolíticos: A terapia combinada é recomendada (a proporção de soluções é determinada pelo tipo de desidratação) | ||||
| Solução de cloreto de sódio 0,9% | 20 -100 ml/kg/dia (dependendo da idade e peso corporal total) IV, gotejamento | Até que o efeito seja alcançado, sob o controle do equilíbrio hídrico e do nível de eletrólitos no soro sanguíneo. | ||
| Soluções de glicose 5%, 10% | a taxa de administração não deve exceder 0,75 g/kg/h IV, gotejamento | |||
| Solução de cloreto de potássio 4%, 7,5% diluída com solução de glicose a 10% + insulina dependendo do volume da solução de glicose | a dose é determinada pela deficiência de potássio no sangue, IV, gotejamento | |||
| Correção da deficiência de micronutrientes: | ||||
| Preparações combinadas de cálcio | 3-4 semanas | |||
| Preparações combinadas de magnésio | ||||
| Correção de hipovitaminose: uma combinação de medicamentos é possível | ||||
| Piridoxina (B1) | 0,02-0,05 g/dia IM | 7 a 10 dias | ||
| Tiamina (B6) | 12,5 mg/dia IM | |||
| Cianocobalamina (B12) | 30 -100 mcg/dia s.c. | |||
| Ácido ascórbico 5% | 1-2 ml por dia IM | |||
| Retinol | crianças com mais de 7 anos de idade 5.000 UI por via oral | dentro de 2-3 semanas | ||
| Raquitismo:(ver protocolo para tratamento de raquitismo) | ||||
| Anemia por deficiência de ferro:(ver protocolo para tratamento de IDA em crianças) | ||||
| Correção de digestão prejudicada: | ||||
| Enzimas pancreáticas microcapsulares | 1.000-2.000 U/kg/dia, por via oral | 7-21 dias | ||
| Correção de distúrbios disbióticos: | ||||
| Probióticos contendo bifidobactérias, lactobacilos | de acordo com a dosagem da idade | dentro de 2 a 4 semanas | ||
Para realizar nutrição parenteral total, a dose de aminoácidos deve ser de 2-2,5 g/kg, gordura - 2-4 g/kg, glicose - 12-15 g/kg. Neste caso, a oferta energética será de 80-110 kcal/kg. As dosagens indicadas devem ser abordadas gradativamente, aumentando a quantidade de medicamentos administrados de acordo com sua tolerabilidade, mantendo a proporção necessária entre substratos plásticos e energéticos (ver algoritmo para criação de programas de PP).
A necessidade energética diária aproximada é de 2 semanas a 1 ano - 110-120 kcal/kg.
A nutrição parenteral é realizada principalmente por via intravenosa. Pelas veias centrais é realizada nos casos em que a NP se destina a ser realizada por mais de 1 semana e quando as veias periféricas estão mal definidas. A utilização da via venosa central é especialmente indicada em pacientes que, juntamente com a NP, necessitam de outras medidas de cuidados intensivos. Para excluir flebite e tromboflebite, soluções concentradas de glicose (› 5%) são infundidas apenas pelas veias centrais. Quando a NP não dura mais de 1 semana, as veias periféricas são proeminentes e são utilizadas soluções isotônicas, dando-se preferência à via periférica de infusão do medicamento. Um fator importante na absorção de fontes nitrogênio-calóricas de PP é o uso simultâneo (por meio de dois conta-gotas paralelos) de misturas de aminoácidos e emulsões gordurosas (ou soluções de glicose). Caso contrário, os aminoácidos também podem ser utilizados para fins energéticos. As emulsões gordurosas não devem ser misturadas com soluções eletrolíticas e medicamentos (devido ao risco de partículas de gordura se unirem). Considerando os casos de reações adversas decorrentes da transfusão de emulsões gordurosas (calafrios, febre, dores no peito, dores lombares, náuseas, vômitos, etc.), o procedimento deve ser realizado durante o dia, na presença de equipe médica. Em alguns casos, se houver intolerância individual ao medicamento, sua infusão é iniciada sob o pretexto da administração intramuscular de um anti-histamínico (suprastin, difenidramina). Eletrólito, componentes de oligoelementos e ácido ascórbico podem ser adicionados a 5; 10; Soluções de glicose a 20%. As vitaminas B são administradas separadamente, por via intramuscular.
A nutrição parenteral pelas veias centrais é realizada após cateterização preliminar de uma das veias de grande calibre, na maioria das vezes a jugular.
Todos os medicamentos devem ser administrados em velocidade mínima (dentro de 22-24 horas), o que garante a máxima absorção das substâncias administradas e reduz significativamente a possibilidade de complicações. As preparações proteicas podem ser misturadas com soluções concentradas de glicose, eletrólitos, vitaminas e microelementos. Não é permitido misturar essas substâncias no mesmo recipiente com emulsões gordurosas.
Algoritmo para compilação de programas PP:
Resolver a questão do uso de medicamentos para terapia de infusão para fins especiais (hemoderivados, plasma, imunoglobulina) e seu volume.
Cálculo da quantidade de soluções eletrolíticas concentradas necessárias à criança, com base na necessidade fisiológica diária e na magnitude da deficiência identificada. Ao calcular a necessidade de sódio, é necessário levar em consideração seu conteúdo em substitutos do sangue e soluções utilizadas para injeções intravenosas a jato.
Determinação do volume da solução de aminoácidos:
Com base no seguinte cálculo aproximado (Tabela 13):
Tabela 13 - Volume de solução de aminoácidos
Determinação do volume da emulsão gordurosa.
No início do uso sua dose é de 0,5 g/kg, depois aumenta para 2,0 g/kg.
Determinação do volume da solução de glicose.
A dose diária de glicose (exceto para recém-nascidos) não deve exceder 6-7 g/kg, mas para garantir eficácia suficiente de carboidratos, sua dosagem não deve ser inferior a 2-3 g/kg por dia. A taxa de utilização da glicose no estado normal é de 3 g/kg/h, e na patologia pode diminuir para 1,8-2 g/kg/h. Esses valores determinam a taxa de administração de glicose - não mais que 0,5 g/kg/h. Para aumentar a utilização da glicose, o uso de insulina na dose de 1 unidade para cada 4-5 gramas de glicose na matéria seca é indicado nos casos em que a glicemia sobe para 10 mmol/l.
No primeiro dia de PN é prescrita solução de glicose a 10%, no segundo - 15%, a partir do terceiro dia - solução de 20% (sob controle de glicemia).
Verificar e, se necessário, corrigir as relações entre substratos plásticos e energéticos. Se houver fornecimento insuficiente de energia por 1 g de aminoácidos, a dose de glicose e/ou gordura deve ser aumentada ou a dose de aminoácidos deve ser reduzida.
Distribuir os volumes resultantes de medicamentos para infusão, com base no fato de que a emulsão gordurosa não se mistura com outros medicamentos e é administrada continuamente ao longo do dia através de um tee, ou como parte de um programa geral de infusão em duas ou três doses em um taxa não superior a 5-7 ml/hora. Soluções de aminoácidos são misturadas com soluções de glicose e eletrólitos. A taxa de sua administração é calculada de forma que o tempo total de infusão seja de 24 horas por dia.
Na realização da PN parcial, o cálculo é feito de acordo com o algoritmo acima, mas levando em consideração o volume do alimento, seu valor energético e o teor de proteínas do leite.
Tratamento medicamentoso fornecido na fase de emergência:
dependendo da causa que levou ao PEM.
· Correção de hipoglicemia;
Tabela 14 - Prevenção/tratamento da hipoglicemia na desnutrição energético-protéica
| Condição da criança | Primeira etapa do tratamento | Tratamento subsequente |
| Se a consciência não estiver prejudicada, mas o nível de glicose sérica estiver abaixo de 3 mmol/l | É indicada uma injeção em bolus de 50 ml de solução de glicose ou sacarose a 10% (1 colher de chá de açúcar para 3,5 colheres de sopa de água) pela boca ou sonda nasogástrica. | Em seguida, essas crianças são alimentadas com freqüência - a cada 30 minutos por 2 horas em um volume de 25% do volume da alimentação única usual, seguida de transferência para alimentação a cada 2 horas sem intervalo noturno |
| Se a criança estiver inconsciente, letárgica ou tiver convulsões hipoglicêmicas | É necessário administrar uma solução de glicose a 10% por via intravenosa a uma taxa de 5 ml/kg. | Em seguida, a glicemia é corrigida com a administração de solução de glicose (50 ml de solução a 10%) ou sacarose por sonda nasogástrica e mudança para alimentação frequente a cada 30 minutos por 2 horas e depois a cada 2 horas sem intervalo noturno. |
A terapia antibacteriana com medicamentos de amplo espectro é indicada para todas as crianças com níveis séricos de glicose alterados.
· Correção de hiper/hipotermia;
Tabela 15 - Prevenção/tratamento da hipotermia na desnutrição protéico-energética (Koletsko B., 2009)
· Correção da desidratação;
Tabela 16 - Realização de terapia de reidratação para deficiência protéico-energética (Bauer K., Jochum F., 1999)
| terapia de reidratação | alimentando | monitoramento de condição | ||
| primeiras 2 horas |
subseqüente 4-10 horas |
após 10 horas de terapia de reidratação |
primeiro 2 horas |
subseqüente 12 horas |
|
se houver sinais de desidratação ou diarreia aquosa, a terapia de reidratação é realizada pela boca ou sonda nasogástrica com solução para reidratação de crianças com PEM (ReSoMal) na proporção de 5 ml/kg a cada 30 minutos durante 2 horas; administrar a mesma solução a 5-10 ml/kg por hora, substituindo a administração da solução de reidratação por alimentação com fórmula ou leite materno às 4, 6, 8 e 10 horas |
a cada 2 horas sem intervalo noturno |
todo 30 minutos |
a cada hora | |
|
- taxa de pulso, - frequência respiratória, - frequência e volume da micção, - frequência de fezes, - frequência de vômito |
||||
· Correção do equilíbrio eletrolítico:
É necessário garantir a ingestão regular de minerais essenciais em quantidades suficientes no corpo da criança. Recomenda-se o uso de potássio na dose de 3-4 mmol/kg por dia, magnésio na dose de 0,4-0,6 mmol/kg por dia. Os alimentos para crianças com PEM devem ser preparados sem sal; apenas a solução ReSoMal é usada para reidratação. Para corrigir distúrbios eletrolíticos, use uma solução mineral eletrolítica especial contendo (em 2,5 l) 224 g de cloreto de potássio, 81 g de citrato de potássio, 76 g de cloreto de magnésio, 8,2 g de acetato de zinco, 1,4 g de sulfato de cobre, 0,028 g selenato de sódio, 0,012 g de iodeto de potássio, na proporção de 20 ml desta solução por 1 litro de alimento.
Outros tipos de tratamento: dependendo da patologia que levou ao PEM.
Cirurgia: para patologias que requerem correção cirúrgica (malformação congênita do trato gastrointestinal, cardiopatia congênita).
Indicadores de eficácia do tratamento:
· aumento adequado dos indicadores de peso e altura;
· eliminação da causa do PEM;
· prognóstico favorável da doença de base que levou ao PEM.
Medicamentos (princípios ativos) utilizados no tratamento
| Albumina humana |
| Ácido ascórbico |
| Bifidobacterium bifidum |
| Dextrose |
| Sulfato férrico |
| Emulsões gordurosas para nutrição parenteral |
| Cloreto de potássio (cloreto de potássio) |
| Colekaltsiferol |
| Complexo de aminoácidos para nutrição parenteral |
| Lactobacilos |
| Levocarnitina |
| Cloreto de Sódio |
| Ácido orótico |
| Pancreatina |
| Piridoxina |
| Retinol |
| Misturas nutricionais enterais |
| Esporos de Bacillus clausii, multirresistentes a vários quimioterápicos e antibióticos |
| Tiamina |
| Tocoferol |
| Ácido fólico |
| Cianocobalamina |
| Sulfato de zinco |
Grupos de medicamentos de acordo com ATC utilizados no tratamento
Hospitalização
Indicações de internação indicando o tipo de internação: (planejada, emergência):
Indicações para internação emergencial e planejada:
· condições de risco de vida devido aos graus PEM II-III;
Indicações para internação planejada:
· esclarecimento da etiologia dos graus PEM II-III (primário ou secundário);
· tratamento de graus PEM II-III, impossível em regime ambulatorial (correção de desequilíbrios hídricos e eletrolíticos, tratamento de infecções, nutrição parenteral, falência de múltiplos órgãos);
· internação em hospital especializado em distúrbios cognitivos.
Prevenção
Ações preventivas:
· atendimento ideal;
· exames médicos regulares;
· nutrição suficiente em frequência e volume, adequada em conteúdo calórico e conteúdo de nutrientes essenciais;
· correção de vitaminas e minerais;
Gestão adicional (após hospitalização):
· expansão da dieta;
· garantir ganho de peso e crescimento;
· estimulação sensorial e apoio emocional;
· reabilitação adicional;
Informação
Fontes e literatura
- Atas de reuniões do Conselho de Especialistas da RCHR do Ministério da Saúde da República do Cazaquistão, 2015
- Lista da literatura utilizada: 1. Nutrição parenteral e enteral: manual nacional / editado por M.Sh. Khubutia, T.S. Popova.-M.: GEOTAR-Media, 2014.- 162-198 p. 2. Guia de Nutrição Clínica. Ed. Lufta VM, Bagnenko SF, Shcherbuka Yu.A. São Petersburgo, 2010. 428 p. 3. Programa nacional para otimizar a alimentação de crianças no primeiro ano de vida na Federação Russa. Ed. Baranova A. A., Tutelyan V. A. M., 2010. 68 p. 4. Dietética clínica da infância. Um guia para médicos. Ed. TE Borovik, KS Ladodo. M.: Medicina, 2008. 606 p. 5. Uglitskikh A.K. Avaliação abrangente do estado nutricional em crianças hospitalizadas // Anestesiol. e ressuscitador. 2005. Nº 2, pág. 52–57. 6. Calder P. C. Ácido graxo ω-3, inflamação e relevância para imunidade para pacientes pós-cirúrgicos e gravemente enfermos // Lipídios. 2004; 39:1147–1161. 7. Mazurin A.V., Vorontsov I.M. Propedêutica das doenças infantis. São Petersburgo, “Foliant”, 2000. - pp. 8. Programa nacional para otimizar a alimentação de crianças no primeiro ano de vida na Federação Russa, Moscou, 2008. 9. Nutrição de uma criança saudável e doente. /Manual para médicos. Editado por Tutelyan V.A., Konya I.Ya., Kaganov B.S. M., 2007.- P 51-52, 60-62. 10. Gastroenterologia pediátrica: guia para médicos / editado por N.P. Shabalov. 2ª ed., revisada - M.: MEDpress-inform, 2013.-187-427 11. Kleiman: Nelson Textbook of Pediatrics, 18ª ed., 2007, Capítulo 43. 12. Sermet-Gauelus I., Poisson-Salomon A. S. , Colomb V. et al. Pontuação simples de risco nutricional pediátrico para identificar crianças em risco de desnutrição // AJCN. 2000. V. 72. R. 64–70. 13. Sawaya A.L., Martins P.A., Martins V.J.B. et al. Desnutrição, saúde a longo prazo e efeito da recuperação nutricional // Nestlé Nutrition Institute. 2009, 63, pág. 95–108. 14. Habilidades práticas do pediatra./Manual para médicos. Editado por Usov I.N. e outros.Mn.: Ensino superior, 1990.- P. 28-39 15. Pediatria: manual nacional / editado por A.A. Baranov. – M., 2009.-165-167p. 16. Collins S, Dent N, Binns P et al., Manejo da desnutrição aguda grave em crianças. www.thelancet.com 2010 17. Transtornos alimentares crônicos em crianças pequenas / editado por R. A. Avdeev, N. L. - Krasnoyarsk: KrasSMA Publishing House, 2008. 18. B. Koletzko, C. Agostoni, P. Ball, V. Carnielli, C. Chaloner, J. Clayton, V. Colomb, M. Dijsselhof, C. Fusch, P. Gandullia e outros. Diretrizes ESPEN/ESPGHAN sobre nutrição parenteral pediátrica. J Pediatr Gastroenterol Nutr, Vol. 41, Supl. 2, novembro de 2005 19. Biesalski HK, Bischoff SC, Boehles HJ, Muehlhoefer A, Grupo de trabalho para desenvolver as diretrizes para nutrição parenteral da Associação Alemã de Medicina Nutricional. Água, eletrólitos, vitaminas e oligoelementos – Diretrizes sobre Nutrição Parenteral, Capítulo 7. GMS Ger Med Sci. 2009;7: Doc21. 4. 20. Fusch C, Bauer K, Böhles HJ, Jochum F, Koletzko B, Krawinkel M, Krohn K, Mühlebach S, Grupo de trabalho para o desenvolvimento das diretrizes para nutrição parenteral da Sociedade Alemã de Medicina Nutricional. Neonatologia/Pediatria – Diretrizes sobre Nutrição Parenteral, Capítulo 13. GMS Ger Med Sci. 2009;7: 21. Fundamentos de nutrição clínica: Materiais de aula para cursos da Associação Europeia de Nutrição Parenteral e Enteral: Trans. do inglês / cap. Ed. L.Sobotka. - 2ª ed. - Petrozavodsk: IntelTek, 2003. - 416 p. 22. Popova TS, Shestopalov AE, et al. Suporte nutricional para pacientes em condições críticas. -M.: LLC "Publishing House" M-Vesti", 2002. - 320 pp. 23. Nutrição parenteral de recém-nascidos: manual clínico\editado por Volodin N.N. - Moscou, 2015 P.27 24.OMS. Manejo da desnutrição grave: um manual para médicos e outros profissionais de saúde seniores. Genebra: OMS 2003 25. Ann Ashworth, Sultana Khanum et al. Diretrizes para o tratamento hospitalar de crianças gravemente desnutridas. Genebra: OMS 2003
Informação
Desenvolvedores:
1) Nazarova A.Z. - Candidato a Ciências Médicas, Chefe do Departamento de Clínica e Diagnóstico do Centro Científico de Pediatria e Cirurgia Pediátrica.
2) Sharipova M.N. - Doutor em Ciências Médicas, Diretor Adjunto de Trabalhos Científicos do Centro Científico de Pediatria e Cirurgia Pediátrica.
3) Adamova G.S. - Candidato a Ciências Médicas, doutor do departamento de somática complexa do Centro Científico de Pediatria e Cirurgia Pediátrica.
4) Litvinova L.R. - farmacologista clínico do JSC National Scientific Cardiac Surgery Center.
Não há conflito de interesses.
Revisor:
1) Khabizhanov B.Kh. - Doutor em Ciências Médicas, Professor do Departamento de Estágio e Residência em Pediatria nº 2 do KazNMU em homenagem a S. Asfendiyarov;
2) Dzhaksylykova K.K. - Doutor em Ciências Médicas, Professor do Departamento de Internato em Pediatria e Cirurgia Pediátrica da Semey State Medical University.
Condições para revisão do protocolo: revisão do protocolo 3 anos após a sua publicação e a partir da data da sua entrada em vigor ou se estiverem disponíveis novos métodos com nível de evidência.
Arquivos anexados
Atenção!
- Ao se automedicar, você pode causar danos irreparáveis à sua saúde.
- As informações publicadas no site MedElement e nas aplicações móveis "MedElement", "Lekar Pro", "Dariger Pro", "Doenças: Guia do Terapeuta" não podem e não devem substituir uma consulta presencial com um médico. Certifique-se de entrar em contato com um centro médico se tiver alguma doença ou sintoma que o preocupe.
- A escolha dos medicamentos e sua posologia devem ser discutidas com um especialista. Somente um médico pode prescrever o medicamento correto e sua dosagem, levando em consideração a doença e o estado do corpo do paciente.
- O site MedElement e os aplicativos móveis "MedElement", "Lekar Pro", "Dariger Pro", "Doenças: Diretório do Terapeuta" são exclusivamente recursos de informação e referência. As informações publicadas neste site não devem ser utilizadas para alterar prescrições médicas sem autorização.
- Os editores do MedElement não são responsáveis por quaisquer danos pessoais ou materiais resultantes do uso deste site.
6237 0
O fornecimento insuficiente de nutrientes e energia dos alimentos (fome parcial ou total) leva ao desenvolvimento de uma condição patológica do corpo, que é indicada em Classificação Internacional de Doenças e Causas de Morte, 10ª revisão (CID-10) Como desnutrição protéico-energética (PEM).
Na literatura médica existem outros termos em relação a esta doença: distrofia nutricional, desnutrição, deficiência de substrato energético, caquexia.
O termo PEM não reflete com precisão a essência do problema, pois junto com a deficiência protéica e energética, via de regra, há deficiência de outros nutrientes (vitaminas, minerais, gorduras, carboidratos).
Causas da desnutrição protéico-energética
Tanto historicamente como atualmente, a subnutrição, na maioria dos casos, tem causas sociais. Estas incluem condições extremas (um exemplo notável é o bloqueio de Leningrado), formas de protesto contra a fome e a pobreza. Várias doenças também contribuem para o desenvolvimento do PEM.Motivos principaisdesnutrição protéico-energética:
1. Fornecimento insuficiente de nutrientes:
A) motivos socioeconômicos, religiosos e outros;
b) causas iatrogênicas (internação hospitalar, jejum por exames, dietas hospitalares, restrições alimentares por doenças diversas, alimentação artificial irracional);
C) distúrbios psiconeuroendócrinos com supressão do apetite e perversão do comportamento alimentar (anorexia neurogênica, psicose);
d) distúrbios mecânicos da ingestão alimentar oral: obstrução gastrointestinal, distúrbios dentários, disfagia;
2. Distúrbios da digestão e/ou absorção de nutrientes: má digestão e síndromes de má absorção.
3. Estados hipercatabólicos:
A) condições em que são liberadas citocinas que aceleram o catabolismo, câncer, febre, infecções;
b) doenças endócrinas com anabolismo prejudicado e catabolismo acelerado (hipertireoidismo, diabetes mellitus).
5. Aumento da perda de nutrientes (distúrbios associados à perda de proteínas e outros nutrientes) síndrome nefrótica, doenças pulmonares obstrutivas crônicas, fístulas intestinais, enteropatia exsudativa, plasmorreia em queimaduras, dermatite descamativa.
6. Maior necessidade de nutrientes:
A) condições fisiológicas (gravidez, lactação, infância e adolescência);
b) condições patológicas (período de convalescença após lesões e doenças infecciosas agudas, pós-operatório).
7. Ingestão de antagonistas de nutrientes no organismo: alcoolismo, intoxicação por antagonistas de vitaminas e medicamentos.
Prevalência de desnutrição protéico-energética
Segundo estimativas da FAO/OMS, no final do século XX, pelo menos 400 milhões de crianças e 0,5 mil milhões de adultos passavam fome no planeta. O seu número aumentou um quarto em 15 anos e a proporção de crianças subnutridas no mundo aumentou no final dos anos 90.O consumo de peixe na Rússia durante o período de 1987 a 1998 diminuiu 2/3; carne, aves e açúcar - em 1/2; salsichas, margarina e manteiga - em 1/3. Estudos seletivos sobre a nutrição da população russa mostraram que cerca de 25% dos pesquisados estão desnutridos e 80% apresentam deficiência de vitaminas e microelementos.
O PEM é um dos principais problemas dos pacientes em hospitais médicos e cirúrgicos. Numerosos estudos demonstraram que mais de 50% dos pacientes que iniciam o tratamento sofrem de deficiência proteico-energética e hipovitaminose grave (especialmente deficiência de ácido fólico, vitaminas B2 e C).
Em 1994, McWriter e Pennington avaliaram o estado nutricional de 500 pacientes em vários departamentos hospitalares do Reino Unido e identificaram PEM em 200 pacientes (40%).

Arroz. 35.1. O estado nutricional dos pacientes em 5 tipos de departamentos, determinado em 100 hospitais do Reino Unido (McWriter, Pennington, 1994): 1 - departamentos cirúrgicos; 2 - departamentos terapêuticos; 3 - departamentos de pneumologia; 4 - departamentos de trauma; 5 - departamentos geriátricos.
De acordo com as clínicas do Centro Russo de Pesquisa Científica da Academia de Ciências Médicas da URSS, o jejum hospitalar entre pacientes com câncer ocorre em 30% dos casos. Entre as pessoas que recebem tratamento ambulatorial para doenças crônicas e câncer, cerca de 10% também apresentam sinais de desnutrição.
O custo da hospitalização para um paciente com estado nutricional normal é aproximadamente 1,5-5 vezes menor do que para um paciente com desnutrição.
Pacientes com desnutrição protéico-energética têm muito mais probabilidade de apresentar atraso na cicatrização de feridas, falha de sutura, aumento da mortalidade, aumento do tempo de hospitalização e recuperação e complicações infecciosas.
Patogênese da desnutrição protéico-energética
A redução da ingestão de nutrientes, independentemente da etiologia, provoca alterações semelhantes. Esta é uma perda não apenas de tecido adiposo e muscular, mas também de tecido ósseo e visceral.O jejum exige que o corpo geralmente economize energia e material plástico. Mas, tal como acontece com o diabetes mellitus dependente de insulina, o jejum completo cria uma situação metabólica de redistribuição de recursos em favor de órgãos e tecidos independentes de insulina. As estruturas dependentes de insulina estão na posição mais desfavorecida. As reservas de glicogênio duram cerca de um dia.
Com um jejum menor, o fígado fornece até 75% de glicose através da quebra do glicogênio. Aumentar a duração do jejum leva a um aumento no nível de gliconeogênese, lipólise e cetogênese. A produção de insulina diminui e o quadro hormonal-metabólico do jejum é fortemente dominado pela ação de um complexo de reguladores contrainsulares.
Nesse caso, são mobilizados os recursos energéticos do componente somático do corpo - músculos esqueléticos e tecido adiposo. A proteína muscular tem um valor energético de cerca de 40.000 kcal. Ocorre um balanço de nitrogênio negativo de 10-12 g/dia, o que indica catabolismo de 75-100 g/dia de proteína. O nível de aminoácidos de cadeia curta (valina, leucina, isoleucina) aumenta no sangue. Neste caso, a perda de mais de 30% da proteína é incompatível com a vida.
Outra fonte potencial de energia é a gordura (130.000 kcal). Aminoácidos e produtos de lipólise são utilizados pelo fígado para ressíntese de glicose e para a formação de corpos cetônicos, a fim de economizar proteínas nos órgãos viscerais e atender às necessidades energéticas do cérebro.
As necessidades energéticas diárias de um homem em repouso após 3-5 dias de jejum requerem o uso de 160 g de triglicerídeos, 180 g de carboidratos (sintetizados pela gliconeogênese) e 75 g de proteína muscular. Assim, as gorduras fornecem a maior parte da energia durante o jejum. Uma pessoa com indicadores nutricionais normais com jejum completo tem reservas próprias suficientes para 9 a 10 semanas.
Durante o jejum, ocorre uma perda desigual de massa nos órgãos individuais, o que foi observado pelos clássicos da ciência da nutrição. Os derivados da mesoderme, assim como os órgãos e tecidos que armazenam carboidratos e lipídios, perdem muito peso. Com um déficit de peso médio no momento da morte de 50-55%, as maiores perdas são observadas no tecido adiposo, reduzidas em quase 99% naqueles que morreram de fome. Há até um desaparecimento de gordura nos lipomas e um desenvolvimento reverso de depósitos lipídicos nas grandes artérias.
O omento e o mesentério tornam-se finas películas de tecido conjuntivo. O epicárdio e a medula óssea amarela são desprovidos de gordura, o que lhes confere uma aparência gelatinosa ou viscosa. Os músculos esqueléticos, que também são dependentes de insulina, reduzem a sua massa em 70%. As alterações atróficas nos órgãos linfóides são muito grandes: o peso do baço diminui em 72%.
A deposição lipocrômica é observada em todos os órgãos atrofiados e a hemossiderose é observada no baço. O fígado perde 50-60% de sua massa, as glândulas salivares - 65%, outros órgãos digestivos - de 30 a 70%. A atrofia mais pronunciada da membrana mucosa do estômago e do aparelho glandular do pâncreas. Nos ossos observa-se osteopatia distrófica com osteoporose e fraturas subperiosteais.
A perda de peso entre o sangue e a pele corresponde aproximadamente à perda relativa total de peso corporal, com atrofia das glândulas da pele, adelgaçamento da epiderme e perda das papilas cutâneas.
Ao mesmo tempo, a atrofia de órgãos vitais independentes da insulina é expressa em muito menor grau. O cérebro, as glândulas supra-renais (especialmente a medula) e os olhos não perdem massa. Nesse caso, a medula espinhal perde mais massa que o cérebro e apresenta mais sinais de alterações degenerativas.
A perda renal em massa é de 6 a 25%, o que é 2 a 9 vezes menor que a média. De acordo com V.D. Zinzerling (1943), os processos atróficos não se espalham para os rins daqueles que morreram de fome. Os pulmões perdem 18-20% da sua massa.
Entre as glândulas endócrinas, a tireoide atrofia especialmente fortemente. Em alguns experimentos, as gônadas quase não perdem peso, e a capacidade sexual de animais famintos, especialmente machos, persiste por muito tempo.
Felizmente, há evidências de que o jejum não tem um efeito esterilizante irreversível. Assim, o médico israelense M. Dvoretsky (1957) relatou fertilidade extremamente elevada em famílias formadas por pessoas que sofreram distrofia nutricional durante o encarceramento em campos de concentração nazistas.
Durante o jejum, o feto fica em posição privilegiada em relação ao corpo da mãe. Embora a desnutrição em mulheres grávidas leve ao nascimento de crianças com desnutrição intrauterina, a perda de peso do corpo materno é muito mais significativa do que a do feto. A nutrição insuficiente das mulheres que amamentam leva à redução e interrupção da lactação e à diminuição do teor de proteínas e gorduras no leite materno.
Formas de desnutrição protéico-energética
Com uma deficiência pronunciada de nutrientes, na maioria das vezes ocorre uma longa fase de compensação, quando os mecanismos endócrino-metabólicos protegem o reservatório de proteínas viscerais e mobilizam gorduras e proteínas do reservatório somático (tecido adiposo e músculos esqueléticos) para as necessidades energéticas. Isso se manifesta na forma de uma forma de fome edematosa ou marântica (marasmo alimentar).No marasmo nutricional (forma mumificada ou seca da distrofia nutricional), a atrofia dos músculos e do tecido adiposo (“pele e ossos”) atinge um grau significativo, mas a pele e o cabelo geralmente permanecem normais, não há alterações na função do fígado e outros órgãos internos, ocorre inchaço. No marasmo, há um excesso significativo dos níveis de glicocorticóides.
Se a deficiência proteica se desenvolver a um ritmo acelerado no contexto do fornecimento do valor energético da desnutrição com a ajuda de hidratos de carbono, então a compensação pode desde o início ser insuficiente em termos de poupança de proteína visceral. Em seguida, desenvolve-se a forma edematosa de jejum (kwashiorkor). A descompensação ocorre mais cedo e os pacientes apresentam taxas de sobrevida mais baixas.
A palavra kwashiorkor vem da língua do povo da África Ocidental que vive onde hoje é Gana. Significa “doença do primogênito após o nascimento do mais novo”. O Kwashiorkor foi descrito pela primeira vez por Williams em 1935 em crianças da África Ocidental alimentadas exclusivamente com milho. Após o desmame, o primogênito fica privado de uma fonte de proteína completa e sua nutrição torna-se insuficiente.
Kwashiorkor, que é uma expressão da deficiência de proteína visceral, é caracterizado por edema, descamação da pele, perda de cabelo, muitas vezes aumento do fígado ou diminuição da função hepática e anorexia. Nesse caso, ocorre hiperaldosteronismo secundário e os efeitos sistêmicos das citocinas são pronunciados.
Alguns casos de fome (desnutrição) podem ocorrer de forma intermediária: a princípio lembra mais a forma de araruta, e com descompensação - a forma kwashiorkor.
Não há uma opinião clara sobre por que uma pessoa está exausta de um tipo ou de outro. De acordo com o ponto de vista tradicional, o marasmo se desenvolve em condições de deficiência predominantemente energética, e o kwashiorkor se desenvolve em condições de deficiência protéica.
As características distintivas dos formulários BEN são apresentadas na Tabela. 35.1. Ambas as formas apresentam sintomas comuns, por exemplo, anemia polideficiente e hipovitaminose.
Tabela 35.1. Formas de desnutrição protéico-energética
| Características distintas | Formulários BEN | |
| Kwashiorkor | Marasmo | |
| Falta | Principalmente proteína | Energia e proteína |
| Aparência | Cara de lua, barriga inchada |
Atrofia dos músculos faciais, bochechas encovadas e fossas temporais. Membros em forma de caule, atrofia da gordura subcutânea e dos músculos esqueléticos. Crescimento atrofiado. O estômago está contraído |
|
Couro e seus derivados |
Manchas de pigmentação anormal e hiperqueratose, “dermatose do esmalte ou descamação”, eritema. Listras de descoloração nos cabelos (sintoma de bandeira) e nas unhas. O cabelo fica mais claro e adquire uma tonalidade avermelhada, fica quebradiço e cai facilmente |
Seco, enrugado, com sinais de poli-hipovitaminose, diminuição do turgor. O cabelo está seco, opaco e fino |
| Comportamento alimentar | Apatia, falta de apetite | Ativo. Apetite presente |
| Fígado | Aumento, dor, esteatose ou esteato-hepatite, ocasionalmente cirrose possível | Atrofia moderada |
|
Trato gastrointestinal |
Mudanças atróficas são menos pronunciadas |
|
|
Metabolismo água-sal |
Edema, ascite, retenção de sódio, hipocalemia, hipofosfatemia, hipomagnesemia |
Sem inchaço. Na fase final da hipercalemia |
| Proteínas do sangue |
Hipoalbuminemia grave, diminuição da transferrina, transtirretina e proteína de ligação ao retinol. Aumento de globulinas de fase aguda Diminuição de VLDL e LDL |
No limite inferior da norma, o VLDL pode aumentar |
| O sistema imunológico |
Imunodeficiência grave de células T e B |
As funções das células T estão predominantemente prejudicadas |
| Fundo hormonal |
Hiperaldosteronismo, altos níveis de citocinas caquéticas, relativamente menos glicocorticóides. A insulina é reduzida. Girotropina é normal. O cortisol é normal. A somatomedina é reduzida |
Níveis extremamente elevados de glicocorticóides, glucagon e somatostatina. A insulina é normal. A tireotropina é reduzida. A triiodotironina é reduzida. A tiroxina está normal ou elevada |
|
Excreção de creatinina |
Aumento moderado | Aumentado acentuadamente |
| Previsão | Pessimista. Alto risco de complicações infecciosas. O tratamento (nutrição) é difícil | Melhor que Kwashiorkor |
De acordo com a Classificação Internacional, as formas de deficiência protéico-energética são diferenciadas apenas em casos graves. Com um grau moderado de PEM com claro predomínio de perda do pool de proteínas viscerais ou somáticas, é aconselhável fazer o diagnóstico da seguinte forma: “Moderada deficiência proteico-energética com tendência ao desenvolvimento de kwashiorkor (marasmo)”.
Complicações da desnutrição protéico-energética
As principais complicações do PEM, que determinam elevada mortalidade e custos de tratamento, são os processos infecciosos.O frequente desenvolvimento de infecções em pacientes com deficiência protéico-energética está associado a uma série de fatores, entre os quais os mais importantes são os distúrbios da resposta adaptativa e a imunodeficiência secundária.
Os distúrbios imunológicos na PEM são caracterizados principalmente pela ruptura do componente das células T. O número absoluto de células T diminui, sua função e diferenciação são prejudicadas.
A função das imunoglobulinas muda. O conteúdo de IgG geralmente aumenta, mas também pode diminuir. Há uma diminuição da IgA e, consequentemente, um enfraquecimento da indução da resposta imune das mucosas à presença do antígeno. Isto se deve à diminuição do número de células produtoras de IgA, à interrupção da síntese dos componentes secretados e à função das células T.
Muitos componentes desempenham um papel na formação da imunodeficiência na PEM (Tabela 35.2).
Tabela 35.2. A relação entre distúrbios nutricionais, função imunológica e suscetibilidade a infecções (de acordo com S. Dreizen., 1979 e R. K. Chandra, 1988)
| Distúrbios de imunidade e resistência | Deficiências nutricionais |
| Imunidade celular |
Proteína, energia, vitaminas B6, B12, ácido fólico |
| Imunidade humoral |
Proteína, vitaminas A, C, PP, B 2, B 6, ácido fólico, pantoteno, biotina |
| Sistema fagocítico-macrófago, interferon, complemento | Proteína, energia, ferro, ácido fólico |
| Barreiras protetoras de tecidos e membranas mucosas |
Proteína, vitaminas A, B2, B6, B12, C, ácido fólico, ferro |
| Regeneração epitelial | Proteína, vitaminas C, zinco |
| Síntese e maturação de colágeno |
vitaminas A, PP, C, B 2, ferro |
| Hematopoiese normoblástica |
Proteína, ferro, zinco, cobre, vitaminas B 12, ácido fólico |
| Coagulação sanguínea | Proteína, cálcio, vitamina K |
A deficiência isolada de certos tipos de nutrientes também pode levar a distúrbios do sistema imunológico. Assim, a deficiência de zinco causa atrofia linfóide, que pode ser detectada pela diminuição da reação de hipersensibilidade do tipo retardada (teste cutâneo com antígeno). Indivíduos com deficiência de ferro ou magnésio podem apresentar um aumento na incidência de doenças infecciosas e testes imunológicos anormais.
A falta de piridoxina, ácido fólico e vitaminas A e E leva a danos ao sistema imunológico celular e à interrupção da síntese de anticorpos. Com a deficiência de vitamina C, a atividade fagocítica dos leucócitos diminui e a função dos linfócitos T diminui.
Diminuição da adaptação na deficiência protéico-energética
Os distúrbios dos sistemas adaptativos são um fator limitante no tratamento dos pacientes, pois estão associados a alterações nas capacidades de diversos sistemas fisiológicos e, quando a nutrição é restaurada, podem levar a estados de desequilíbrio e alterações nas necessidades nutricionais.Um ponto importante na redução da adaptação pode ser a diminuição da atividade da bomba de sódio, responsável por 30% do gasto energético do corpo em repouso completo. Uma diminuição na sua atividade leva a alterações no gasto energético dos tecidos e à perturbação das relações eletrolíticas intracelulares. Nesse caso, ocorre uma diminuição da labilidade do sistema de condução do coração, da capacidade dos rins de concentrar a urina e diminui o peristaltismo. trato gastrointestinal (TGI).
Outra razão para o gasto energético basal está relacionada ao catabolismo protéico. No PEM, o conteúdo intracelular ácido ribonucleico (ARN), peptídeos, enzimas. As perdas de aminoácidos e íons estão associadas à cinética das proteínas, que são utilizadas como fonte de energia.
A próxima função adaptativa interrompida está relacionada à resposta inflamatória e à resposta imune. As lesões cutâneas não são dolorosas, não incham e não ficam vermelhas. Em caso de pneumonia, o exame radiográfico não revela infiltração maciça. As infecções do trato urinário ocorrem sem piúria. Sinais de febre, taquicardia e leucocitose podem ser amenizados. Quando exausto, a função termorreguladora fica prejudicada.
Problemas clínicos decorrentes do PEM: atrofia muscular, diminuição da função respiratória e termorreguladora, fraturas, escaras, diminuição da taxa de cicatrização de feridas, comprometimento da função imunológica e hormonal, aumento da incidência de complicações pós-operatórias, diminuição da resistência a infecções, depressão e muitos outros.
Anteriormente, são apresentados os principais indicadores utilizados na prática clínica para avaliar o grau e a forma da desnutrição protéico-energética. Uma diminuição predominante nos parâmetros antropométricos caracteriza a exaustão do tipo marasmo; uma diminuição pronunciada nos marcadores laboratoriais do pool de proteínas viscerais (albumina, transferrina) caracteriza o kwashiorkor. Os parâmetros imunológicos pioram em ambas as formas da doença.
Atenção especial deve ser dada aos marcadores de proteínas viscerais, uma vez que seu nível (principalmente albumina) se correlaciona com a mortalidade e o desenvolvimento de complicações.
Ao trabalhar com pacientes debilitados, é necessário tratar todos os dados laboratoriais e de exames instrumentais com cautela. Praticamente não existe área de atividade do corpo que não seja afetada pelo PEN.
Freqüentemente, médicos inexperientes têm dificuldade em interpretar os resultados dos testes e sua dinâmica nesses pacientes. É preciso lembrar que podem variar muito dependendo do grau de hidratação e podem ser muito elevados antes do início do tratamento (infusões). Para avaliar a dinâmica, paralelamente a quaisquer análises é necessário avaliar o hematócrito.
Nutrição terapêutica para deficiência protéico-energética
O tratamento do PEM deve ser realizado em uma determinada sequência. A primeira tarefa é compensar deficiências nutricionais específicas e tratar complicações como infecções, distúrbios da microflora intestinal e restauração das funções adaptativas. No futuro, uma dieta deverá ser desenvolvida para restaurar a perda de tecido. O objetivo final é normalizar a composição corporal.Escolhendo o método de tratamento preferidoA desnutrição protéico-energética é determinada por dois fatores principais:
1) grau e forma do BEN;
2) etiologia do PEM.
Muitos especialistas acreditam que a administração de nutrientes por infusão intravenosa é perigosa porque pode facilmente ultrapassar o limiar quando a capacidade de homeostase está prejudicada. A nutrição parenteral completa ou predominante é indicada principalmente nos casos em que a causa inicial da deficiência protéico-energética foram doenças associadas à má absorção ou hipercatabolismo. Também é utilizado no desenvolvimento de complicações do PEM.
Ao utilizar nutrição parenteral durante a fase inicial do tratamento para PEN, é importante não administrar excesso de proteínas, calorias, líquidos e eletrólitos. A administração de nutrientes através do trato gastrointestinal permite que o intestino seja usado como uma barreira entre o médico e o metabolismo do paciente, portanto o tratamento da desnutrição protéico-energética requer o uso máximo do sistema digestivo sempre que possível.
Na gênese alimentar do PEM, a nutrição parenteral é prescrita para pacientes com doença grave na forma de kwashiorkor com alterações distróficas pronunciadas no trato gastrointestinal paralelamente ao início da nutrição enteral. Em caso de exaustão na forma de marasmo, bem como graus moderados de PEM, são prescritas misturas enterais. Dependendo da situação, utiliza-se o acesso por sonda ou a administração oral do medicamento (beber lentamente com canudo).
Em caso de deficiência protéico-energética grave, é aconselhável utilizar misturas balanceadas de meio elemento; em caso de grau moderado, podem ser prescritos meios poliméricos padronizados ou misturas hipernitrogênicas hipercalóricas.
Uma forma leve de PEM é geralmente compensada por uma dieta suave com alto teor de proteínas e energia (em condições instituições médicas e preventivas (HCI)- dieta rica em proteínas).
Deficiências específicas de vitaminas e minerais devem ser corrigidas com tratamento ativo. Normalmente é necessária a prescrição de ferro, magnésio, cálcio, fósforo, zinco, ácido fólico e vitamina A. Segundo nossas observações, muitas vezes há necessidade do uso de ácido nicotínico para o alívio da pelagra.
É considerado prudente administrar proteínas e calorias em quantidades próximas das necessidades aos pacientes cujas deficiências específicas foram corrigidas e cujas infecções foram curadas. Para alcançar o equilíbrio positivo de nitrogênio e energia necessário para a reparação dos tecidos, é necessário aumentar a quantidade de nutrientes.
Na maioria dos pacientes, isso é possível devido ao retorno do apetite e ao aumento da ingestão de alimentos por via oral. Porém, em alguns pacientes é necessário aumentar a nutrição parenteral.
Em nossa opinião, deve-se respeitar os limites inferiores das normas recomendadas, uma vez que a ingestão elevada de proteínas (até 2,0 g/kg) muitas vezes não corresponde a capacidades metabólicas prejudicadas para sua absorção.
Os critérios para a eficácia do tratamento são o balanço positivo de nitrogênio e o aumento dos indicadores nutricionais, principalmente do peso corporal. Porém, em pacientes com kwashiorkor, nos primeiros dias de tratamento, o peso corporal, via de regra, diminui devido à eliminação do edema hipoalbuminêmico, passando a aumentar aproximadamente 100-150 g/dia.
A reabilitação de pacientes está frequentemente associada a um aumento desproporcional do peso corporal (não devido às proteínas, mas devido ao tecido adiposo), o que requer maior correção da composição corporal.
Um problema especial é o PEM, que se desenvolveu como resultado da anorexia nervosa. Neste caso, a nutrição terapêutica é ineficaz sem influência psicoterapêutica. Os pacientes, geralmente meninas, concordam com as recomendações dietéticas do médico, mas induzem secretamente o vômito após comer, tomam laxantes e imitam a baixa tolerância às soluções de nutrição parenteral. Esse comportamento é causado pelo medo da obesidade ou do excesso (do ponto de vista do paciente) de peso corporal.
Na fase inicial, a intervenção psicoterapêutica deve ter como objetivo:
Superação da atitude anosognósica em relação à doença, resistência óbvia ou oculta ao tratamento;
- correção das ideias do paciente sobre o peso corporal ideal;
- correção das ideias do paciente sobre formas de controlar e manter o peso corporal.
Muitos pacientes com deficiência protéico-energética subestimam a gravidade de sua condição e recusam a hospitalização. Infelizmente, às vezes os médicos ambulatoriais não avaliam adequadamente a situação, mesmo com PEM grave, e não insistem na internação urgente. PEN moderada e grave, especialmente com diminuição do pool de proteínas viscerais, deve ser tratada em ambiente hospitalar!
A atenção do paciente deve ser chamada para a natureza potencialmente fatal dos distúrbios somatoendócrinos associados à perda de peso. O paciente deve compreender que o principal indicador de recuperação é a restauração do peso corporal.
Nas fases iniciais do tratamento, a dieta alimentar deve ser rigorosamente regulamentada. O comportamento nutricional dos pacientes é monitorado pela equipe de enfermagem. Os pacientes mantêm um diário de auto-observação no qual registram a ingestão diária de alimentos, horário e situação de alimentação.
Em uma coluna especial, é anotado o estado psicoemocional (sentimentos, emoções, pensamentos, comportamento) durante as refeições. É importante que a equipe médica e os familiares condenem o comportamento alimentar patológico e, por outro lado, elogiem e encorajem os sucessos alcançados no tratamento.
A.Yu. Baranovsky
Nutrição adequada e nutritiva - Condição necessaria para o crescimento e desenvolvimento normais do bebê.
Porém, há situações em que há deficiência de macro ou microelementos no corpo do bebê. Isto leva a vários tipos consequências negativas, atrasos no desenvolvimento físico e intelectual.
Falaremos sobre as causas e o tratamento da desnutrição protéico-energética em crianças no artigo.
O que devo alimentar meu filho se ele for alérgico ao leite em pó? Descubra mais sobre isso no nosso.
Conceito e características

A desnutrição protéico-energética é uma condição patológica causada por falta de macroelementos do grupo de proteínas.
Essa condição pode se desenvolver rapidamente, por exemplo, durante períodos de jejum, quando o bebê não recebe nutrição adequada e rica em proteínas.
O PEM também pode ocorrer gradativamente, caso haja problemas no funcionamento do trato gastrointestinal, acompanhado de absorção de proteínas prejudicada.
Causas
Podemos falar de um processo patológico no caso em que o peso corporal da criança diminui rapidamente, o bebê perdeu peso nos últimos 6 a 12 meses. perdi mais de 5-10% do meu peso.
Vários fatores negativos podem levar a esse fenômeno, como:
- Nutrição pobre, causada por uma série de motivos, como, por exemplo, condições econômicas desfavoráveis da família, necessidade de seguir uma dieta rigorosa para fins terapêuticos, fatores religiosos, lesões no aparelho mandibular, que levam à impossibilidade de ingerir alimentos naturalmente . Vários tipos de anomalias psicológicas, em particular a anorexia, também podem levar a distúrbios alimentares.
- Doenças, interrompendo o processo de digestão e absorção de proteínas. Essas doenças incluem câncer, diabetes mellitus e distúrbios do trato gastrointestinal.
- Risco de desenvolver PEM aumenta durante a adolescência Quando os níveis hormonais de uma criança mudam, observa-se um rápido crescimento e desenvolvimento do corpo. Nessa situação, o adolescente necessita de mais nutrientes e, se não forem fornecidos em quantidade suficiente, desenvolve-se a patologia.

Quem está em risco?
Na maioria das vezes, o PEM ocorre em crianças que vivem em condições desfavoráveis, quando a criança não há oportunidade de comer plena e adequadamente. O PEM freqüentemente se desenvolve em crianças e adolescentes.
Como uma criança tem alergia ao glúten? descubra agora mesmo.
Patogênese
A deficiência de macronutrientes é uma condição que o corpo deve se adaptar. Durante o processo de adaptação, vários tipos de mudanças são notados nele. Essas alterações estão relacionadas principalmente aos níveis hormonais e à atividade do sistema endócrino.
Outros órgãos internos também sofrem porque não recebem nutrição suficiente para o seu funcionamento normal.
Para normalizar a situação, o corpo redistribui aminoácidos do tecido muscular e adiposo para outros órgãos que precisam deles.
Como resultado, desenvolve-se o principal sintoma do PEM – perda de gordura e massa muscular. Há uma desaceleração nos processos metabólicos e uma perda acentuada de peso corporal.
Na fase inicial perda de peso é muito significativa(4-5 kg por semana), esses números diminuem ligeiramente, mas o peso corporal continua a diminuir, embora não tão rapidamente.
Classificação e etapas

Existem 2 formas principais de BEN:
- marasmo. Há retardo de crescimento, atrofia da gordura subcutânea e do tecido muscular;
- kwashiorkor. O quadro clínico, neste caso, é complementado por problemas no funcionamento do fígado (acumulam-se elementos gordurosos em suas células, que normalmente não deveriam estar presentes), e a criança apresenta inchaço. A condição da gordura subcutânea permanece inalterada.
Dependendo da gravidade do curso, distinguem-se várias formas de patologia:
- Leve 1º grau.É caracterizada por enfraquecimento do corpo, diminuição da imunidade e aumento da fadiga. A criança cansa-se rapidamente, sente-se sonolenta e muitas vezes recusa jogos ao ar livre.
- 2º grau moderado. Há uma defasagem em altura e peso. A criança é mais suscetível a vários tipos de vírus e infecções e muitas vezes fica doente, pois o sistema imunológico muda no nível celular.
- Grau severo. Há um atraso pronunciado na altura, peso e fraqueza do tecido muscular, que é especialmente perceptível nas extremidades. Existem distúrbios no funcionamento do trato gastrointestinal. Isso se manifesta na forma de diarréia e dor abdominal após comer. O cabelo da criança começa a cair gradativamente, a qualidade da pele e das unhas piora. O metabolismo dos fluidos nos tecidos do corpo é perturbado, o que leva ao desenvolvimento de edema.
- Forma isolada. Neste caso, estamos falando de níveis insuficientes de numerosos micro e macroelementos essenciais no corpo.
É interrompido o funcionamento dos órgãos internos que, sem receber nutrientes suficientes, não conseguem desempenhar suas funções normalmente.
Possíveis complicações e consequências

Deficiência proteico-calórica – condição perigosa para a saúde da criança, o que pode levar a diversas consequências adversas.
Esses incluem:
- diminuição persistente da imunidade, a formação de uma resposta imunológica inadequada a irritantes. Isto leva a doenças infecciosas frequentes, muitas das quais podem causar danos significativos à saúde e ao desenvolvimento;
- (as crianças geralmente têm deficiência de vitaminas B e A). Isso pode causar ressecamento da pele, aparecimento de manchas senis, alterações nas membranas mucosas do corpo e desenvolvimento de processos inflamatórios. Desenvolvem-se distúrbios nervosos, como apatia, depressão e distúrbios do sono. Além disso, a deficiência de vitaminas leva a a ocorrência de vários tipos de doenças(conjuntivite, glossite, leucopenia e muitas outras);
- com PEM é possível distúrbio do metabolismo mineral, o que leva a problemas no sistema músculo-esquelético (por exemplo, osteoporose);
- a função cardíaca está prejudicada, outros órgãos internos.
Sintomas e quadro clínico
As manifestações da patologia podem ser diferentes. Em primeiro lugar, este depende da gravidade da doença. Assim, com deficiência protéico-energética leve, o quadro clínico é mal expresso, a criança queixa-se principalmente de mal-estar e fraqueza.
Se o PEM for mais grave, o quadro clínico é mais variado. Aqui principais características que caracterizam o PEN:

Diagnóstico
O diagnóstico da doença é feito em etapas. Em primeiro lugar, doutor avalia a condição física do paciente de acordo com critérios como:
- indicadores de altura e peso;
- avaliação de indicadores físicos e emocionais (atenção, velocidade de reação, frequência de doenças infecciosas, etc.);
- avaliação da condição da pele;
- tônus muscular (com PEM é reduzido);
- avaliação do desenvolvimento da camada de gordura subcutânea;
- avaliação da alimentação da criança (realizada semanalmente).
Testes laboratoriais obrigatórios:

Pesquisa Adicional:
- imunograma;
- teste genético;
- exames de hardware.
Você encontrará informações sobre o tratamento da síndrome astênica em crianças em nosso site.
Tratamento
O principal objetivo terapêutico do PEM é a normalização dos processos metabólicos do corpo, quando a oferta de nutrientes é superior ao seu consumo. Além de uma dieta nutritiva, é prescrito à criança repouso (para patologias graves - repouso no leito), além de manter-se aquecido.
A alimentação da criança deve consistir principalmente de alimentos ricos em elementos de fácil digestão.
As refeições devem ser fracionadas, ou seja, o número de refeições é de 5 a 6 vezes ao dia, o tamanho da porção é pequeno. Você precisa comer esses alimentos Como:

É importante lembrar que a alimentação deve ser o mais suave possível, mas não menos completa. Grandes refeições não são recomendadas a quantidade de alimentos consumidos deve corresponder às normas para a idade e peso da criança. A principal condição é uma alimentação variada, rica em micro e macroelementos.
Previsão
A deficiência protéico-energética é uma condição que pode levar à morte (segundo as estatísticas, a taxa de mortalidade entre crianças que sofrem da patologia é de 5 a 40%).
Tudo depende da gravidade da doença, de suas manifestações clínicas e também de Quão competente foi o tratamento prescrito?.
Prevenção

O desenvolvimento do PEM pode ser evitado se as seguintes regras forem seguidas:
- Comportamento correto(boa alimentação, ausência de maus hábitos, descanso suficiente) para a gestante durante o período de gravidez.
- Amamentação pelo maior período possível, introdução oportuna de alimentos complementares.
- Se a criança for alimentada com mamadeira, mais Monitore cuidadosamente os ganhos de altura e peso.
- Fortalecendo o sistema imunológico, organizando uma rotina diária e dieta adequada.
O PEM em uma criança pode levar não apenas ao retardo físico, mas também ao retardo mental no desenvolvimento. Além disso, esta condição é fatal para o bebê, uma vez que os órgãos e sistemas internos de seu corpo não são capazes de desempenhar normalmente suas funções na ausência de uma nutrição normal.
Pedimos gentilmente que não se automedique. Marque uma consulta com um médico!